- Giỏ của bạn trống trơn
- tiếp tục mua hàng
Noggin là một protein hoạt tính sinh học được dùng trong các ứng dụng nuôi cấy tế bào. Protein Noggin liên kết với các phối tử của họ TGF-β và điều chỉnh hoạt động của chúng bằng cách ức chế khả năng tiếp cận các thụ thể truyền tín hiệu của chúng. Noggin ban đầu được xác định là chất đối kháng BMP-4 có tác dụng quan trọng đối với sự hình thành thích hợp của đầu và các cấu trúc lưng khác.
Trình tự:
MQHYLHIRPAPSDNLPLVDLIEHPDPIFDPKEKDLNETLLRSLLGHYDPGFMATSPPEDRPGGGGGAAGGAEDLAELDQLLRQRPSGAMP
SEIKGLEFSEGLAQGKKQRLSKKLRRKLQMWLWSQTFCPVLYAWNDLGSRFWPRYVKVGSCFSKRSCSVPEGMVCKPSKSVHLTVLRWRC
QRRGGQRCGWIPIQYPIISECKCSC với thẻ polyhistidine ở đầu C
Nguồn:
Escherichia coli
Thuốc thử và phòng thí nghiệm không có động vật
Được sản xuất và thử nghiệm theo hướng dẫn GMP
Mức độ nội độc tố:
<0.1 EU trên 1 μg protein theo phương pháp LAL.
Hoạt động:
Đo bằng khả năng ức chế sản xuất phosphatase kiềm do BMP-4 gây ra bởi tế bào ATDC5.
ED50 đối với hiệu ứng này là <0.05 μg/mL khi có 50 ng/mL BMP-4 tái tổ hợp của con người.
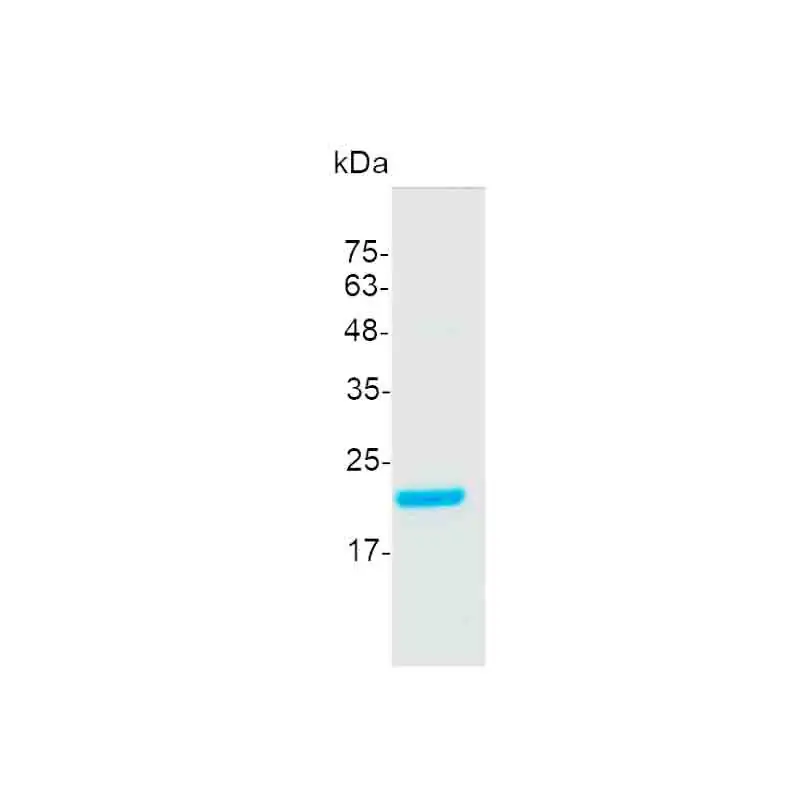
Độ tinh khiết:
>98% được xác định bằng SDS-PAGE. Được tinh chế bằng sắc ký Ni-NTA.
Công thức:
Protein được đông khô từ dung dịch chứa 1X PBS, pH 7.4.
Tái tạo:
Nên tái tạo protein đông khô trong H vô trùng2O đến nồng độ không dưới 100 μg/mL và ủ dung dịch gốc trong ít nhất 20 phút để đảm bảo dung dịch được hòa tan trở lại đủ.
Lưu trữ:
Protein đông khô nên được bảo quản ở nhiệt độ -20°C. Sản phẩm này ổn định trong một năm sau khi nhận được, khi được xử lý và bảo quản theo hướng dẫn. Sau khi hoàn nguyên, các phần protein nên được bảo quản ở nhiệt độ -20°C hoặc -80°C. Tránh các chu kỳ đông lạnh/rã đông lặp lại.
Lưu ý:
Vui lòng sử dụng trong vòng một tháng sau khi hoàn nguyên protein.
Đặc điểm kỹ thuật:
Protein tái tổ hợp Croyez GMP® được sản xuất tại cơ sở đạt chứng nhận ISO 13485:2016 và GMP.
Các quy trình bao gồm:
● Kiểm tra và truy xuất nguồn gốc nguyên liệu
● Hồ sơ bảo trì và hiệu chuẩn thiết bị
● Hồ sơ đào tạo nhân sự
● Tính nhất quán giữa các lô
● Tài liệu về kiểm soát QA và thay đổi quy trình
● Được sản xuất và thử nghiệm theo hệ thống quản lý chất lượng được chứng nhận ISO 13485:2016
● Giám sát độ ổn định của thời hạn sử dụng sản phẩm
Tham khảo:
1. Krause, C. và cộng sự (2011) Int J Bioool Biol. 43,4: 478-81.
2. Que, J. và cộng sự (2006) Phân biệt. 74,7: 422-37.