- 您的購物車是空的
- 繼續購物


間質幹細胞 (MSC) 是成體多能細胞,已被證明具有非凡的抗癌特性,使其成為癌症治療的獨特選擇。研究人員目前正在探索利用間質幹細胞進行癌症治療的新方法,例如裝載抗癌藥物,或改造間質幹細胞來運輸藥物化合物。然而,值得注意的是,間質幹細胞在癌症治療中的作用存在爭議,應予以考慮。
大多數抗癌藥物可以被間質幹細胞從培養環境中吸收,這使得它們成為潛在的抗癌藥物。 藥物輸送車輛 在癌症治療中。這導致了藥物啟動 MSC 的簡單方法的開發,例如將它們與紫杉醇、吉西他濱或索拉非尼等藥物一起孵育,這些藥物已被證明可以被 MSC 有效吸收。然而,應該指出的是,藥物吸收到 MSC 中的途徑可能因藥物類型而異。有些藥物透過轉運蛋白吸收,而有些藥物則依靠簡單的擴散或內吞作用。這凸顯了了解 MSC 吸收不同藥物的特定機制的重要性,因為這可能會影響它們作為癌症治療中藥物傳遞載體的有效性。
用於生產癌症治療精準藥物的間質幹細胞最重要的治療機制之一是其腫瘤歸巢能力。這項特性允許將多種抗癌藥物標靶遞送至腫瘤部位。到達腫瘤後,間質幹細胞能夠以時間依賴性方式釋放抗癌藥物。藥物釋放的有效性由細胞類型和藥物類型共同決定。例如,研究表明,載藥人類骨髓間質幹細胞 (hBM-MSC) 1 小時後開始以 2 pg/細胞的速度釋放紫杉醇,1.7 小時後增加至 2.0-144 pg/細胞。另一方面,脂肪組織來源的間質幹細胞(AD-MSCs)被發現在前 48 小時內釋放大部分紫杉醇,而在隨後的 144 小時內僅釋放少量。
間質幹細胞選擇性地針對腫瘤並以受控方式釋放藥物的能力為開發更有效和更精確的癌症治療帶來了重大希望。
間質幹細胞有潛力成為 被基因工程處理過 表達或分泌一系列可以抑制癌症生長和進展的化學物質。使用基因工程 MSC 可以遞送三類藥物:治療蛋白、自殺基因和溶瘤病毒。
首先,許多研究已提出治療性蛋白質的遞送。 MSC 可以傳遞治療性蛋白質,如生長因子、細胞激素、幹擾素和轉錄因子,以抑制腫瘤生長或作為促腫瘤因子的抑制劑。其中一種細胞激素是 IL-12,它可以增加 T 細胞和細胞毒性 NK 細胞的活化。研究表明,表達 IL-12 的 MSC 可以減少腎細胞癌和子宮頸腫瘤小鼠模型中的腫瘤生長。 IFN-β 等乾擾素與腫瘤特異性抗體或標準化療藥物合併使用時,已被證明可以有效限制小鼠模型中的癌症進展。許多研究也顯示轉錄因子是有益的。例如,表達促凋亡蛋白腫瘤壞死因子相關凋亡誘導配體(TRAIL) 的MSC 已被證明可以促進多種惡性腫瘤(包括肺癌、乳腺癌、腦瘤、子宮頸癌和結直腸腫瘤)中腫瘤細胞的凋亡。 。
其次,間質幹細胞經過基因改造,表達自殺基因,能夠將無害的試劑轉化為有毒的抗癌藥物。這種方法的原理是,轉基因間質幹細胞可以在腫瘤附近將前藥轉化為活性形式,從而選擇性殺死癌細胞。幾種酵素前藥系統已用於各種類型的腫瘤,包括單純皰疹病毒胸苷激酶與更昔洛韋複合(HSV-TK/GCV系統)、CD與5-氟胞嘧啶(5-FC)、 CE與伊立替康(CPT- 11),以及細胞色素 P450 與環磷醯胺或異環磷醯胺。例如,攜帶「自殺基因」胞嘧啶脫氨酶::尿嘧啶磷酸核糖轉移酶(CD::UPRT)的間質幹細胞可有效減少腫瘤生長。 CD::UPRT能夠將無毒藥物5-氟胞嘧啶轉化為有毒抗腫瘤劑5-氟尿嘧啶,已被證明對結腸癌和黑色素瘤小鼠模型有效。
最後,溶瘤病毒(OV)可以透過表面蛋白識別和黏附癌細胞來選擇性殺死癌細胞,從而導致溶瘤。 OV 有多種,包括腺病毒、皰疹病毒、麻疹病毒、柯薩奇病毒、小兒麻痺病毒、呼腸孤病毒、痘病毒和新城疫病毒。例如,溶瘤單純皰疹病毒-1已被證明可以透過減少抗發炎巨噬細胞的比例和增加腫瘤浸潤淋巴細胞的比例來改變腫瘤微環境(TME)。然而,直接OV遞送的功效通常是有限的,因為宿主的防禦機制可以去除外源病毒。因此,MSC 被用作運輸和保護 OV 的載體。
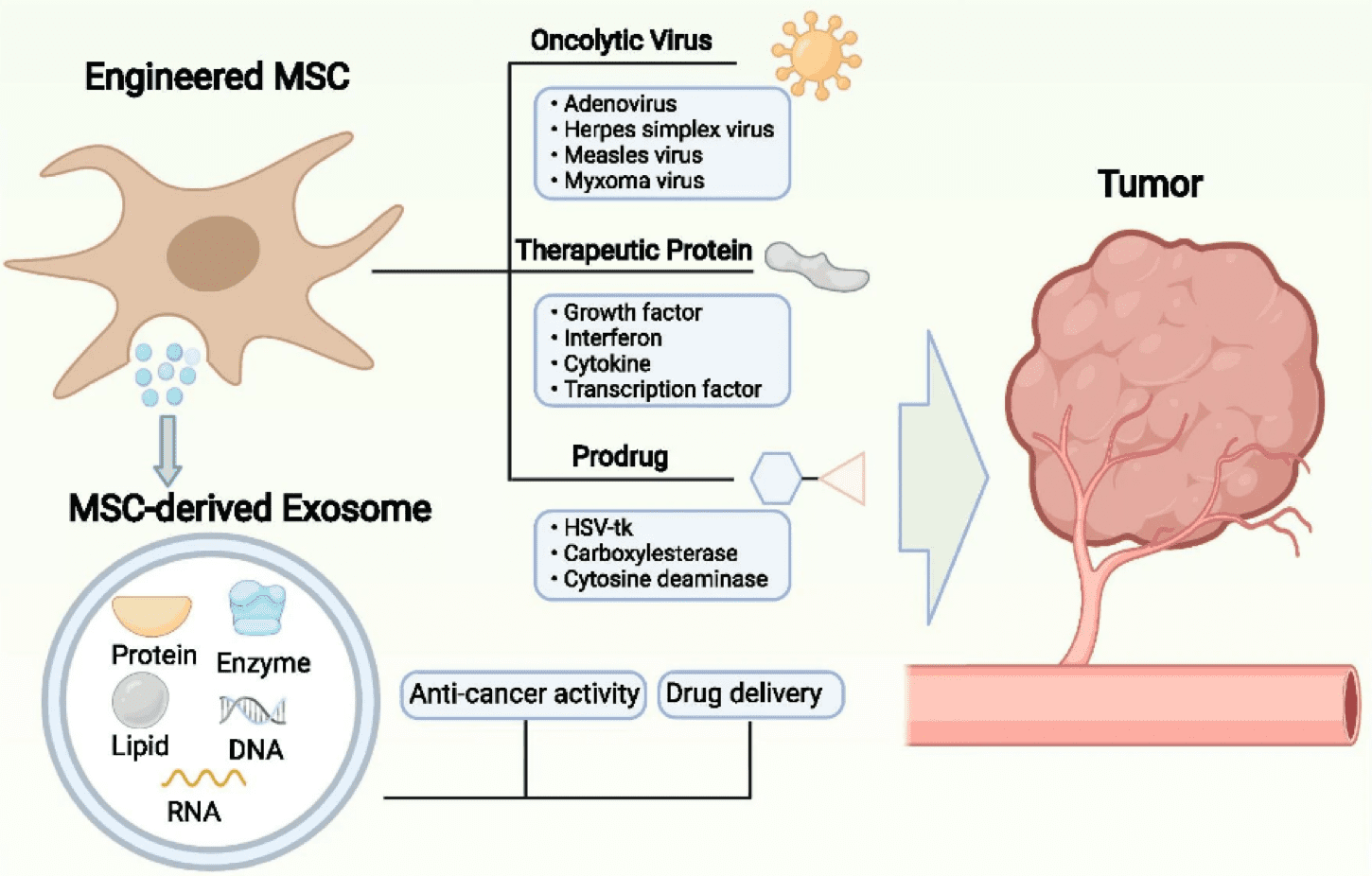
圖片來源:Lan T、Luo M、Wei X doi:10.1186/s13045-021-01208-w 轉載於 知識共享許可
間質幹細胞的免疫調節特性是透過直接的細胞間相互作用或可溶性物質的旁分泌釋放來介導的。然而,有幾個 有爭議的 MSC 角色 應該要提到這一點,特別是它們對癌症進展的影響。
一方面,間質幹細胞可能以多種方式在癌症的形成和進展中發揮作用。例如,MSC 可以透過釋放 CCL5 等物質來影響腫瘤細胞的表型,從而促進轉移性乳癌細胞的侵襲性。此外,間質幹細胞透過上調乳癌和前列腺惡性腫瘤 TME 內 VEGF 和 IL-6 的表達水平,從而與腫瘤血管生成相關,從而導致腫瘤血管化增加。此外,為了回應癌細胞產生的可溶性物質(如 TGF-1),間質幹細胞可能發育成癌症相關纖維母細胞(CAF)。最後,除了透過可溶性訊號分子顯示促腫瘤特徵外,MSC還可以透過細胞間接觸或細胞吞噬直接促進腫瘤發展。
另一方面,大量研究發現MSCs透過MSC對腫瘤細胞的細胞毒性來抑制腫瘤的發生和進展。例如,先前的研究表明,MSC 透過 PI3K/AKT 途徑引起細胞凋亡並減少神經膠質瘤細胞增殖。此外,細胞間接觸導致 MSC 將淋巴癌的細胞週期停止在 G0/G1 期。
MSC 抑製或增加癌症形成的能力可能會受到實驗條件(例如動物模型、細胞系、劑量和治療持續時間)差異的影響。因此,有必要進行進一步的體內研究來系統性地研究MSC的這些作用。
總而言之,雖然使用載藥或基因工程間質幹細胞治療癌症有許多有前景的方法,但也存在一些必須解決的潛在問題。首先,腫瘤細胞根除後殘留的修飾間質幹細胞可能會產生不可預見的問題。其次,間質幹細胞傳遞的治療蛋白可能會影響間質幹細胞的增殖並增加畸胎瘤形成的機會。第三,MSC腫瘤歸巢的功效可能會因歸巢分子表現不足而受到影響,這可能會導致脫靶問題。因此,研究人員有一個重要的機會繼續完善基於間質幹細胞的癌症治療技術,以最大限度地減少這些問題並最大限度地發揮其治療潛力。
Babajani A、Soltani P、Jamshidi E、Farjoo MH、Niknejad H。載藥間質幹細胞與抗腫瘤藥物用於癌症標靶治療的最新進展。前沿生物工程生物技術。 2020;8:748。
Harrell CR、Volarevic A、Djonov VG、Jovicic N、Volarevic V。間質幹細胞:抗腫瘤免疫中的朋友或敵人。國際分子科學雜誌。 2021;22(22):12429。
Hemminki O、Dos Santos JM、Hemminki A。用於癌症免疫治療的溶瘤病毒。 J Hematol Oncol。 2020;13(1):84。
Lan T, Luo M, Wei X. 間質幹/基質細胞在癌症治療的應用。 J Hematol Oncol。 2021;14(1):195。
梁文,陳X,張S,等。間質幹細胞作為腫瘤生長的雙面刃:關注 MSC 衍生的細胞激素。細胞分子生物學快報。 2021;26(1):3。
Marofi F、Vahedi G、Biglari A、Esmaeilzadeh A、Athari SS。間質基質/幹細胞:基於細胞的癌症標靶基因治療的新時代。前免疫學。 2017;8:1770。


了解細胞治療新創公司如何利用關鍵製程參數 (CPP) 來確保產品品質、有效擴展規模並符合監管標準。
