基于外泌体的疗法监管路线图:FDA、EMA 和东盟指南

基于外泌体的疗法监管路线图:FDA、EMA 和东盟指南
- 亚特兰蒂斯生物科学
- 博客
- 阅读时间: 10 分钟
细胞分泌的微小细胞外囊泡——外泌体,激发了全球生物技术创新者的无限遐想。它们富含蛋白质、脂质、RNA和其他生物活性分子,在靶向药物递送、再生医学以及治疗从神经系统疾病到癌症等多种疾病方面展现出巨大的潜力。对于生物技术初创公司而言,外泌体产品的商业化之路令人振奋,但也充满了监管方面的重重障碍。
截至10月2025, 目前尚无任何基于外泌体的疗法获得FDA批准。强调了严格遵守规定的必要性。

FDA和EMA如何监管外泌体疗法?
1. 美国FDA监管框架
分类
- 用于治疗用途的外泌体产品受到监管。 毒品 根据《联邦食品、药品和化妆品法案》(FD&C 法案)和 生物制品 根据《公共卫生服务法》第 351 条。
- 属于再生医学范畴,特别是同种异体应用(例如,来自间充质干细胞或羊水的外泌体)。
- 最小操作(定义于 21 CFR 1271.3(f))是指不改变细胞或组织相关生物学特性的处理(例如,不进行工程改造的基本分离)。
- 大多数治疗性外泌体(例如,经工程改造携带RNA/蛋白质载荷或用于非同源功能的外泌体) 不会 经过最小程度的处理,并作为药品/生物制品受到监管。 第351, 需要IND/BLA。
- 只有经过最小程度处理的、拟用于同源用途且符合其他标准(例如,无全身性影响)的HCT/P才能受到监管。 《公共卫生服务法》第361条这种方式要求较低,而且 无需经过药物审批程序即可商业化 “351”产品必需。
非微加工产品的上市前要求
- 尽管 FDA 尚未发布专门的“外泌体治疗产品指南”,但制造商必须遵守生物制品生产途径,并遵守适用于生物制品的化学、生产和控制 (CMC) 和良好生产规范 (GMP) 要求。
- 需要 研究性新药 (IND) 临床试验申请,包括详细的安全性和有效性数据。
- 需要一个 生物制品许可证申请(BLA) 为获得市场准入许可,需进行严格的质量、安全性和有效性评估。
监管监督:
- 目前,尚无针对外泌体疗法的具体监管指南。然而,现有的细胞和组织类产品标准可为非临床和临床开发过程中外泌体疗法的表征提供有益的指导。
- 受FDA指南约束 化学、制造和控制 (CMC) 适用于生物制品的要求。
2. 欧盟EMA监管框架
分类
- 基于外泌体的疗法可分为以下几类: 先进治疗药品 (ATMP) 根据(EC)第1394/2007号条例,如果符合特定标准:
- 含有具有明确治疗作用机制(例如基因沉默、组织修复)的功能活性货物(例如 mRNA、miRNA 或蛋白质)。
- 经过大量改造(例如基因改造、加载治疗剂或进行广泛纯化)或用于非同源功能(即与天然作用不同的功能)。
- 可归类为 基因治疗药物, 体细胞疗法药品 或 联合 ATMP (例如,将外泌体整合到医疗器械中)。
- 外泌体 未进行实质性操纵 并用于 同源功能 (例如,经过最少加工以达到天然免疫调节效果) 不会 符合ATMP标准,并可能受到监管。 指令2001 / 83 / EC 或其他国家框架。
审批流程
- ATMP分类的外泌体需要 集中式市场授权程序 通过 欧洲药品管理局(EMA)包括临床前和临床数据,以证明安全性、有效性和质量。
- 此 先进疗法委员会(CAT) 评估 ATMP 分类,制造商可以要求进行正式的分类程序以获得更清晰的分类结果。
- 分类需视具体情况而定,取决于操纵程度和预期用途。
根据美国FDA和EMA的要求,产品制造商必须确保符合以下规定: 良好生产规范(GMP) 并解决批次间差异和免疫原性等挑战。
国际监管框架的协调,特别是 FDA 和 EMA 之间的协调,在简化基于外泌体的疗法的全球商业化方面发挥着至关重要的作用。
许多东盟国家遵循美国FDA和EMA的指导方针以达到全球标准,但各成员国的具体要求有所不同。遵守FDA严格的第351条标准和EMA的ATMP框架有助于在全球范围内拓展市场。
3. 新加坡卫生科学局(HSA)
- HSA在其CTGTP框架中并未明确列出外泌体。然而,基于外泌体的疗法是 可能作为细胞、组织或基因治疗产品 (CTGTP) 进行监管 当他们是 经过大幅改造、用于非同源功能、被改造并负载治疗性载荷或以异体方式给药.
- 反过来, 经最小程度改造的、用于自体同源功能的胞外囊泡可能不受CTGTP调控。须经新加坡卫生科学局(HSA)的产品分类评估。
- 建议尽早与 HSA 联系以确认分类。
- CTGTP 要求包括:
- 根据操作方式和预期用途进行产品分类(类似于FDA 351/EMA ATMP 的依据)
- 根据临床试验授权 (CTA) 提交的临床试验的 IND 等效申请
- 符合生物制品生产PIC/S标准的GMP合规性
4. 泰国食品药品监督管理局(TFDA)
- 根据泰国食品药品监督管理局的监管框架,基于外泌体的疗法将被合理地视为 生物药品 (或先进疗法产品)根据《BE 2510 药品法》的规定,须遵守 GMP、临床试验授权和质量监管,如同细胞和基因疗法一样。
- 然而,目前尚无公开的泰国食品药品监督管理局(FDA)指南明确对外泌体进行分类。
- 强烈建议与泰国食品药品监督管理局就产品分类进行讨论。
旨在将外泌体产品商业化的科学家应尽早与监管机构接洽,以明确产品分类,确保在满足严格的安全性、质量和功效标准的同时,高效地完成跨地区的临床试验和市场授权流程。
初创公司如何构建符合GMP规范的外泌体产品线
商业化始于监管策略。以下是专为初创企业量身定制的分阶段方法:
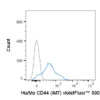
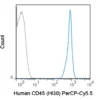
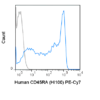
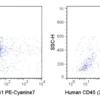
- IND 前准备开展全面的临床前研究,以确定其安全性和作用机制。积极参与FDA的INTERACT或pre-IND会议,以便尽早获得关于CMC计划的反馈。注重标准化:使用经验证的检测方法进行外泌体的分离、纯度测定(例如,外泌体含量>95%)和表征(大小、标记物等)。 CD63/CD81).
- IND 申请提交IND申请以启动临床试验。申请中应包含详细的生产方案、质量控制措施和风险评估。GMP合规性是不可妥协的。如果公司内部生产能力有限,则应与合同生产组织(CMO)合作。
- 临床开发:遵循良好临床规范(GCP)进行试验设计,重点关注患者安全和数据完整性。通过MedWatch监测不良事件,并根据中期结果进行调整。
- BLA通路为获得市场准入许可,需提交生物制品许可申请(BLA),并提供充分的数据证明其安全性和有效性。获批后,需持续开展药物警戒和标签合规工作。
IND模块3:外泌体疗法的化学、生产和控制(CMC)
外泌体产品必须遵守FDA针对生物制品和基因疗法制定的CMC(化学、制造和控制)指南中概述的全面标准,这些标准同样适用于细胞外囊泡(EV)。这包括在IND申报文件(模块3)中提供详细的文件,涵盖原料药(DS)和制剂(DP)的生产、分析方法和稳定性数据。
关键要素包括验证制造工艺 原材料控制、外泌体制备、分离、浓缩和表征,以确保一致性、纯度和效力, 确保从实验室到GMP级别的可重复性和可扩展性。
基于风险的方法对于解决 EV 异质性至关重要,验证过程可利用单囊泡分析等先进分析方法确认货物封装效率和表面修饰。
在开发基于细胞外囊泡(EV)或外泌体的治疗产品时,关注杂质(包括外泌体自身产生的杂质和外源杂质)对于安全性、免疫原性和监管合规性至关重要。初创公司应尽早优先考虑GMP合规性,包括各项控制措施。 防止污染 以及 对动物源性材料中外来因素的评估。
目前已知的基于细胞外囊泡的疗法存在两个主要安全隐患:
(1)电动汽车自身的安全性和
(2)共分离杂质和污染物带来的风险.
尽管细胞外囊泡(EVs)具有治疗益处,但它们也参与疾病的发生发展。例如,肿瘤来源的EVs可以促进癌症进展,如果不能完全清除,还可能引发意想不到的不良反应。因此,在研发和生产过程中,必须严格控制来源细胞和EV的异质性。
第二类风险源于 外来因素和工艺衍生杂质,包括 支原体、病毒、内毒素、培养基添加剂(例如血清成分)和残留的生产试剂因为这些污染物会引发免疫或毒理反应,所以需要采取强有力的措施。 质量控制体系 至关重要。
阅读更多关于 外泌体疗法中质量控制至关重要。
EV制剂也可能含有 非预期电动汽车子类型, 退化的EV变体和 非电动汽车颗粒 例如脂蛋白、蛋白质聚集体和实验室器皿中的人工微粒。许多此类颗粒的大小与细胞外囊泡 (EV) 相似,一旦引入细胞外囊泡就极难分离。因此, 通过制造设计进行预防性控制 至关重要。采用针对表面电荷或分子标记的净化策略,并尽量减少可能引入空气传播颗粒物的开放式操作步骤。
为了降低污染风险, 无异种成分、化学成分明确的培养基 以及 不含动物源性成分的试剂 建议使用人源或动物源性原材料。这些原材料会增加病毒传播的可能性,并可能引入意想不到的生物活性(例如,使用胎牛血清时可能引入牛源细胞外囊泡)。质量控制策略应包括以上两方面。 定性和定量杂质分析,定义 接受限度和 效价指标已根据粒子数进行归一化 检测杂质稀释。
残留抗生素和培养基成分可能导致 过敏反应或炎症反应缓解措施包括在 GMP 生产过程中消除不必要的添加剂,同时在开始对人体给药时进行适当的临床风险管理和提高患者/研究人员的意识。
总而言之,最大限度地减少杂质负担并彻底表征 EV 成分对于确保产品安全、控制免疫风险和获得监管部门批准至关重要。
除了基础的临床前研究之外,还应重点关注外泌体的特性表征(例如,表面标志物等)。 CD63、CD81、CD9)、组成(蛋白质、RNA、脂质)、粒径(30–100 nm)、纯度(>95%)以及通过合格检测方法测定的效力。在IND申报文件中,应包含生物分布、免疫原性和治疗功能的机制细节,以支持作用机制。
结语
| 类别 | 主要要求/注意事项 | 目的/影响 |
|---|---|---|
| 生产验证 | 验证 原材料控制, 隔离, 分割, 浓度和 特性 流程。 | 从研发到GMP规模,保证产品的可重复性、纯度和效力。 |
| 基于风险的方法 | 地址 EV异质性 并确认 货物封装 以及 表面改性 利用单囊泡分析技术。 | 支持治疗的一致性和可预测性。 |
| 主要安全风险 | 1. 细胞外囊泡本身的安全性(例如,肿瘤来源的细胞外囊泡) 2. 来自……的风险 共分离的杂质和污染物. | 防止免疫原性和意外的生物学效应。 |
| 潜在污染物 | 支原体、病毒、内毒素、血清衍生囊泡、蛋白质聚集体、脂蛋白和实验室器皿微粒。 | 污染可能引起免疫反应或中毒反应。 |
| 控制策略 | - 实施 封闭系统工作流程 - 使用 表面电荷或基于标记的纯化 尽量减少开放式操作。 | 降低颗粒交叉污染的风险。 |
| 媒体和试剂 | 绝大部分储备使用 无异种成分、化学成分明确的培养基 以及 不含动物源性成分的试剂避免胎牛血清污染。 | 防止病毒传播和意外生物活性。 |
| 质量控制(QC) | 包括 定性+定量杂质分析,定义 接受限度并将效力正常化 粒子计数. | 确定产品一致性和纯度阈值。 |
| 残余成分 | 监测并消除 抗生素, 中级补充剂以及残留试剂。 | 最大限度减少过敏反应和炎症反应。 |
| 分析表征 | 评估 身份识别(CD63、CD81、CD9), 组成成分(RNA、蛋白质、脂质), 尺寸(30–100 纳米), 纯度(>95%), 效力和 协议备忘录. | 在IND申报文件中证明产品质量和作用机制。 |
| 总体的目标 | 建立一个您自己的 符合GMP标准、特性明确的EV治疗药物 具有明确的杂质控制措施和经过验证的CMC文件。 | 有助于获得监管部门批准并实现安全的临床转化。 |
初创公司能从FDA警告信中学到什么
FDA警告信清晰地指明了什么。 不会 待办事项。过去五年,该机构已多次向未经批准销售外泌体产品的公司发出信函,强调其屡次违规行为。
截至2025年10月,美国FDA已就外泌体产品发布了12份警告信。以下是主要内容:
- 未经批准的营销和未经证实的声明
许多公司在缺乏临床证据或FDA批准的情况下,宣传外泌体可用于治疗阿尔茨海默病、帕金森病、自身免疫性疾病、新冠肺炎、癌症和伤口愈合等严重疾病。此类宣传使产品成为“未经批准的新药”,并可能导致虚假宣传指控。应避免夸大其词的营销;在临床试验验证疗效之前,应坚持使用临床前数据。
- 缺乏适当的许可和合规性
产品未经生物制品许可申请 (BLA) 或研究性新药申请 (IND) 即被分销,且往往无视现行药品生产质量管理规范 (CGMP)。问题包括无菌保证不足、标签不规范以及未注册为HCT/Ps(人源细胞制品/塑料制品)。
- 无视事先通知和安全报告
尽管收到未具名的信函或检查,多家公司仍继续运营,导致警告级别升级。一些公司报告了严重不良事件,例如因产品污染导致患者住院,促使FDA发布公共安全通告。
- 同种异体使用及给药风险
缺乏安全性数据的静脉注射、关节注射、雾化或局部用药产品上市已被列为禁忌。初创企业必须优先进行严格的免疫原性和传播风险测试。
这些发现凸显了FDA的立场,即外泌体产品在上市前需要经过严格的审批流程,尤其是用于人类治疗用途的产品。公司通常需要在15个工作日内做出回应,并提出纠正措施。
美国食品药品监督管理局 (FDA) 向不合规公司发出的警告信,结合监管指南和行业最佳实践,可以帮助初创科学家了解在将外泌体产品推向市场时需要注意的事项。通过了解这些要素,初创科学家可以避免代价高昂的错误,并建立一条合规的成功之路。这些警告信并非仅仅是惩罚性的,它们也具有教育意义。在 FDA 网站上查阅这些警告信有助于预先了解可能受到的审查。
外泌体初创公司的最佳实践

除了规章制度之外,成功还取决于卓越的运营:
- 质量控制和标准化对原材料(例如细胞来源)和生产工艺实施严格控制。采用可扩展的生物制造工程方法,确保批次间的一致性。诸如以下工具: 可调谐电阻脉冲传感 (TRPS) 流式细胞术是必不可少的。
- 原材料和试剂管理:选用符合GMP标准的细胞系或组织,并进行无菌和功能测试控制,以最大程度地减少变异性。对于负载型外泌体,需验证预负载(例如,在生产细胞中进行重组表达)或分离后技术,并评估动物源性赋形剂(如传染性海绵状脑病)带来的风险。
- 确保批次间一致性实施标准化的细胞外囊泡(EV)生物合成、摄取和稳定性方案,并通过效力测定和可追溯性验证批间一致性。通过遵守GMP规范和国际标准(如ISEV指南)来解决细胞培养条件等生产因素的影响。
- 尽早与FDA沟通以应对CMC不确定性利用 INTERACT 会议讨论影响关键质量属性(例如纯度、稳定性)的产品变更。维护详细的批次记录和标准操作规程 (SOP),以便在生产规模扩大时进行审核和可比性研究。
- 知识产权与合作关系尽早为专有分离方法或工程化外泌体申请专利。与学术机构合作获取临床前数据,并与合同生产商合作进行GMP规模化生产。
- 道德营销即使在临床前阶段,也应避免在网站或社交媒体上暗示其具有治疗功效。而应着重强调其科学潜力。
- 最新资讯:通过FDA的再生医学页面关注其最新动态并订阅提醒。积极参与行业组织,例如…… 国际细胞外囊泡学会(ISEV) 寻求同行的见解。
优先考虑安全和患者疗效
安全至关重要。FDA的信函强调了未经测试的产品可能造成的危害,包括感染和免疫反应。应开展全面的毒理学研究,并报告所有不良事件。对于初创企业而言,建立透明的企业文化有助于赢得监管机构和投资者的信任。
Atlantis Bioscience:在东南亚发现电动汽车GMP解决方案
在亚特兰蒂斯生物科学公司,我们与初创公司、衍生公司和生物企业家合作,将外泌体创新转化为实际应用。 符合GMP标准的治疗药物电动汽车产品的商业化不仅需要卓越的科学技术,还需要精准的监管——而这正是我们擅长的领域。我们的团队提供 端到端支持从细胞外囊泡 (EV) 的分离和表征,到 CMC 文件编制和符合 GMP 标准的工艺开发,我们提供全方位服务。通过整合经验证的分析平台、无污染试剂以及符合 FDA、EMA 和 PIC/S 标准的质量控制策略,我们助力确保您的外泌体疗法达到纯度、效力和重现性方面的最高标准。
凭借在新加坡、泰国以及更广泛的东盟市场积累的深厚区域经验,Atlantis Bioscience 能够弥合监管和技术方面的差距,这些差距往往会延缓临床转化,从而助力您从 从长凳到床边 有信心。
结论:合规性是一种竞争优势

将外泌体疗法商业化需要耐心和精准,但其带来的回报——满足未被满足的医疗需求的变革性疗法——是值得的。通过吸取警告信中的教训并遵循FDA的指导,生物技术初创公司可以有效地应对这一复杂的局面。请记住,合规并非障碍,而是可持续创新的基石。尽早咨询监管专家,您的外泌体产品可能成为生物技术领域的下一个突破。欲了解最新信息,请访问 FDA资源 直。
案例
- https://www.fda.gov/drugs/therapeutic-biologics-applications-bla/frequently-asked-questions-about-therapeutic-biological-products
- www.novavitalabs.com/post/what-is-a-361-vs-351-product-understanding-fda-regulation-of-human-cells-and-tissues
- EMA关于临床试验中研究性先进疗法药品质量、非临床和临床要求的指南(参考编号:EMA/CAT/22473/2025)
- https://www.hsa.gov.sg/ctgtp/regulatory-overview
- Takakura Y 等人。基于细胞外囊泡的治疗产品的质量和安全性考虑因素。药物研究。2024
- https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/compliance-actions-and-activities/warning-letters
- https://www.isev.org/
CONTACT
您可能喜欢的其他博客


ExoBrite™ 为何优于 PKH 和碳菁染料
2025 年 10 月 7 日
探索超越PKH的可靠EV标记。探索Biotium的ExoBrite™染色剂,实现准确、可重复的细胞外囊泡分析。