- 您的購物車是空的
- 繼續購物
CRISPR-Cas9基因編輯 徹底改變了生物醫學研究,為修改 DNA 提供了前所未有的精確度。然而,將 CRISPR 組件有效且安全地遞送到目標細胞中仍然是一個主要障礙。 腺相關病毒(AAV) 由於其安全性、組織特異性和長期基因表達,已成為領先的運載工具。
CRISPR-Cas9 是突破性的基因編輯工具,最初源自於細菌中的天然免疫防禦系統。它徹底改變了基因工程,因為它 精確, 效率以及 多功能性.
CRISPR-Cas9 是一個雙組分系統:
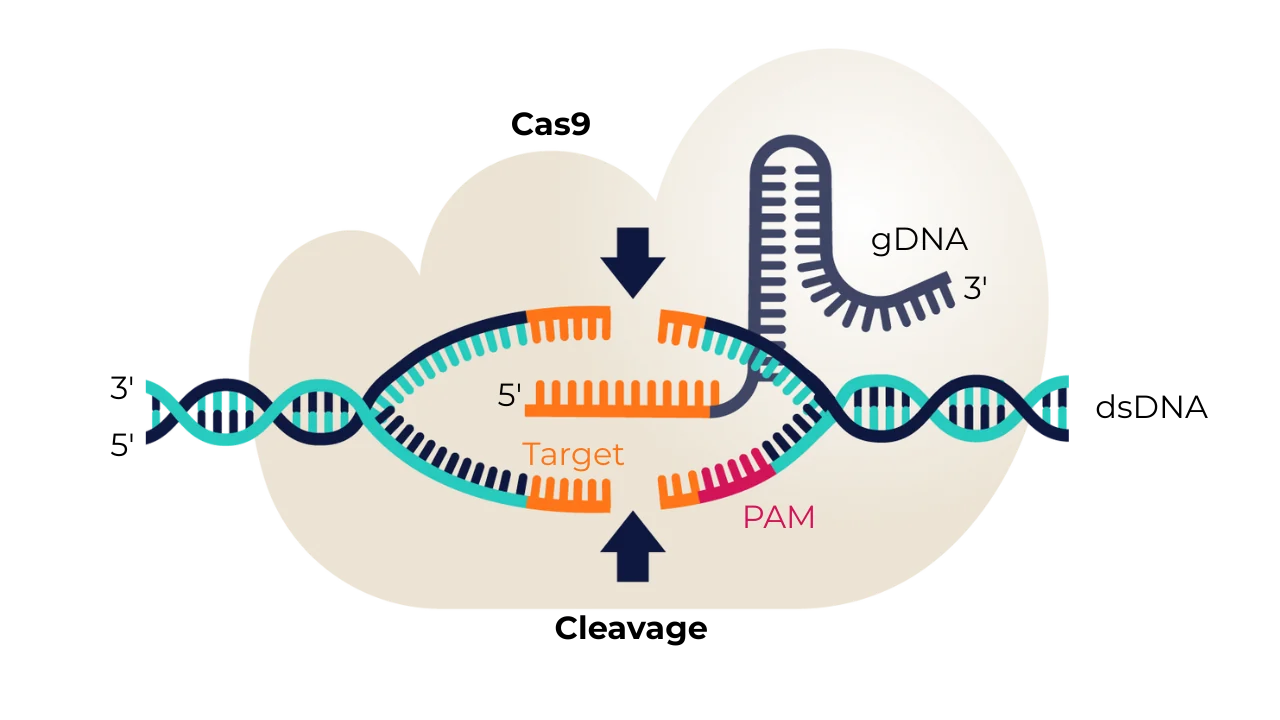
Cas9 切割 DNA 後,細胞會將斷裂檢測為損傷並迅速激活其自然修復系統。修復途徑的選擇決定了DNA是簡單地修補錯誤還是精確地重寫,這對於基因組編輯的結果至關重要。
1.非同源末端連接(NHEJ)
2. 同源性定向修復(HDR)
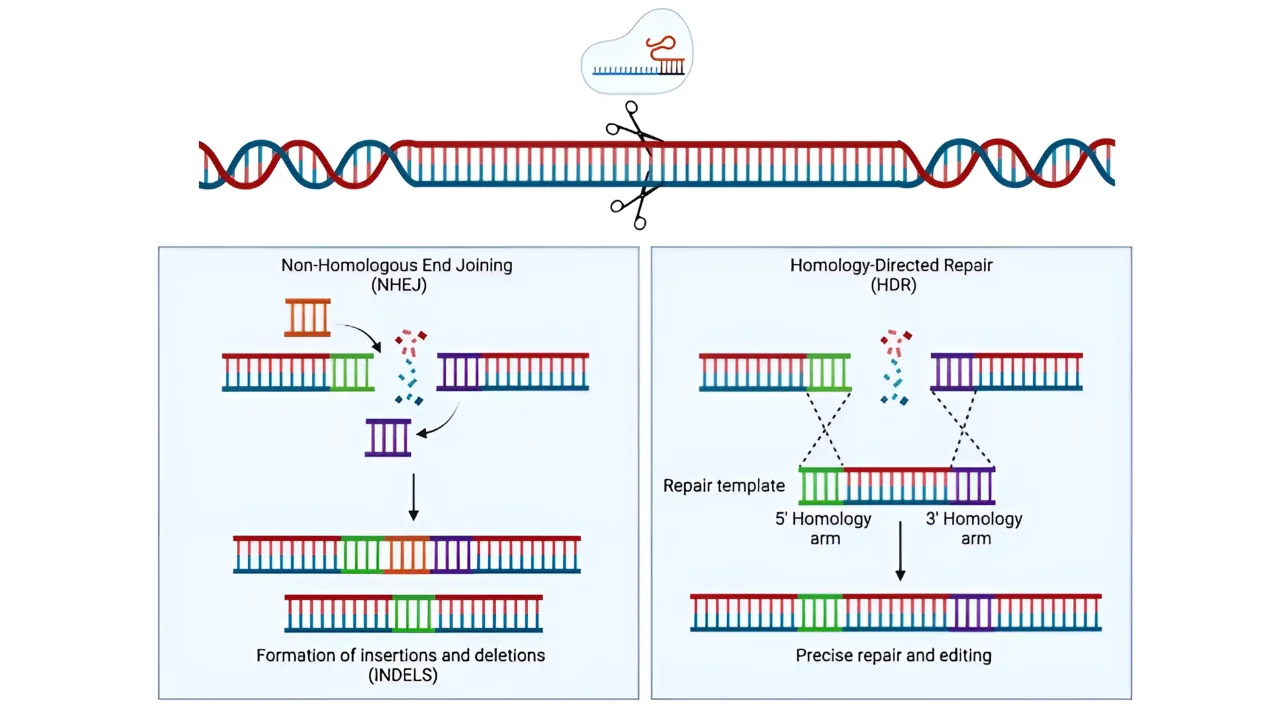
將 CRISPR 組件有效地遞送到細胞中對於成功進行基因組編輯至關重要。在眾多運送方法中,AAV 已成為一種流行的選擇。
AAV 非常適合 CRISPR 遞送,因為它們:
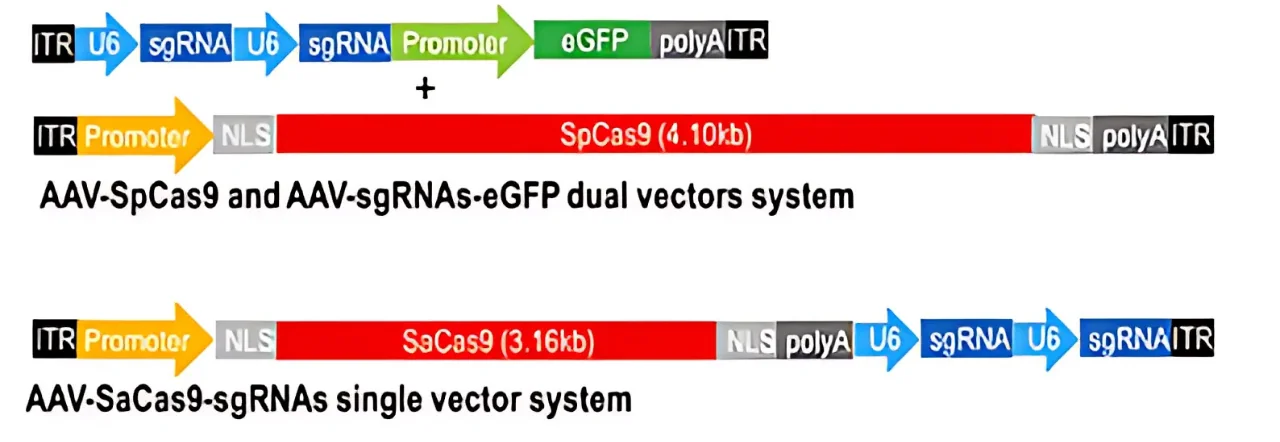
雖然 AAV 是 CRISPR 遞送的高效載體,但它們的載貨能力相對較小,約為 4.7 千鹼基(kb)。 這使得將 Cas9 蛋白和 sgRNA 裝入單一 AAV 變得頗具挑戰性。例如, SpCas9 (從 化膿性鏈球菌),即第一個被廣泛使用的 Cas9 酶,相對較大(~4.2 kb),幾乎沒有空間容納必需的調控元件和引導 RNA。一種更小、與 AAV 更相容的 Cas9 酶, SaCas9 (從 金黃色葡萄球菌),後來被認為是一種有前途的替代方案,由於其尺寸較小(~3.2 kb),具有更容易包裝到 AAV 載體中的優勢。
為了克服 AAV 的尺寸限制,已經開發出幾種創新策略和方法:
AAV 是 CRISPR 傳遞的廣泛選擇,因為它們能夠有效傳導多種細胞類型,同時保持低免疫原性。然而,優化 AAV 傳遞需要幾個關鍵工具和策略來確保有針對性和有效的基因組編輯。這些策略專注於增強組織特異性表達、gRNA 設計、修復模板傳遞和對 Cas9 活性的時間控制。
總之,這些工具和策略為 AAV-CRISPR 傳遞提供了關鍵的增強,確保基因編輯過程對於各種治療應用既有效又安全。
| 項目類別 | 關鍵工具/元素 | 標註/優點 |
|---|---|---|
| 發起人 | • 普遍存在:CAG、EF1α • 肝臟特異性:TBG、ApoE • 神經元:突觸蛋白、CaMKIIα • 肌肉特異性:MHCK7、Desmin | 組織特異性表現;減少脫靶活性 |
| gRNA設計 | • U6、H1啟動子(Pol III) • 多重 gRNA | 高效定位;支持複雜的基因組編輯 |
| 修復模板 | • 供體 DNA 共遞送 • 雙AAV HDR策略 | 精確編輯(例如點突變或插入) |
| 可調控系統 | • 藥物誘導型 Cas9(例如 Tet/Dox) • 自失活 Cas9 系統 | 時間控制;降低脫靶和免疫風險 |
在體內 基因組編輯涉及將 CRISPR 組件直接遞送到生物體中,從而實現系統性或組織特異性的修改,而無需 離體 細胞操作。 AAV 尤其 非常適合這種方法 因為它們能夠有效地針對特定組織。
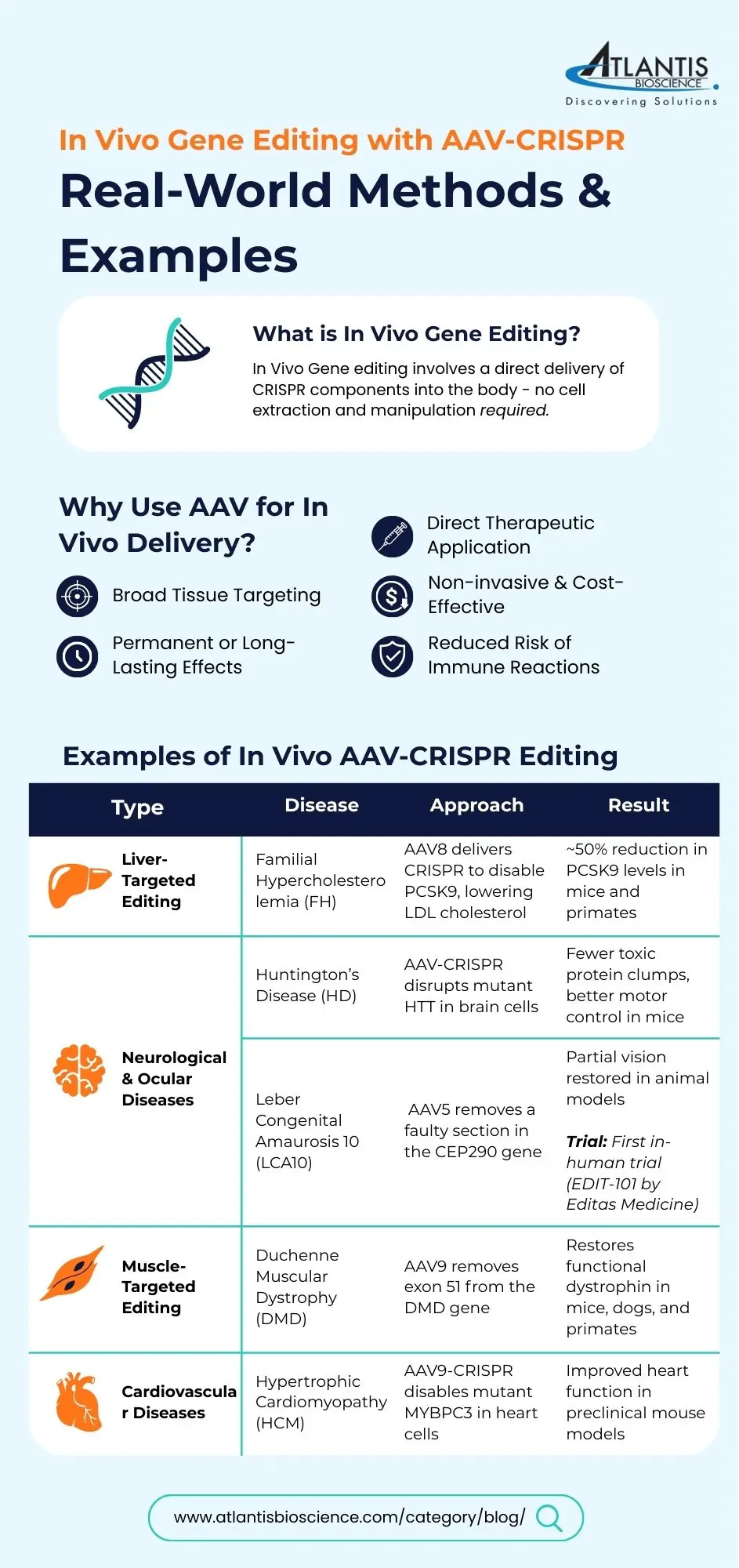
儘管 体内 AAV-CRISPR 基因編輯仍存在一些技術和轉化挑戰。克服這些障礙對於充分發揮基因組編輯對多種疾病的治療潛力至關重要。持續創新 向量設計、編輯技術和製造流程正在塑造該領域的未來方向,旨在提高臨床應用的安全性、有效性和可及性。
AAV 介導的 CRISPR 遞送是一種有效的策略 体内 基因組編輯,提供精確度、組織特異性和長期效果。雖然包裝限制和免疫反應等挑戰仍然存在,但微型編輯器、分裂系統和可調節 Cas9 的創新正在推動該領域的發展。
臨床試驗(例如 LCA101 的 EDIT-10)證明了 AAV-CRISPR 療法在現實世界中的潛力。隨著研究的進步,我們可以期待在直接治療患者遺傳疾病方面取得更多突破。
PackGene生物技術 已成為 AAV 載體設計、製造和 CRISPR 相關治療開發的領導者。它們同時提供 客製化 AAV 服務 以及 即用型 CRISPR/Cas9 rAAV 產品 顯著加速 体内 基因編輯研究。
PackGene 的現成 CRISPR/Cas9重組腺相關病毒 產品旨在提供高品質、可靠的結果,並具有快速的周轉時間,以確保您的專案順利推進。無論您需要廣泛表達還是組織特異性靶向,我們預製的 AAV 都可滿足您的體內基因組編輯需求。
了解我們 產品目錄 今天或 聯繫我們的團隊 討論我們如何幫助您實現下一次突破!

了解 LNP 配方中的四種基本脂質——可電離脂質、磷脂質、膽固醇和 PEG 脂質——以及它們如何驅動高效的 RNA 遞送。
探索 AAV、LNP 和外泌體如何促進神經基因治療,並利用影像工具提高中樞神經系統標靶治療的精確度。

探索在亞洲選擇 AAV 生產 CDMO 的關鍵標準。了解如何確保基因治療的成功,確保品質、可擴展性和監管專業知識。