- 您的購物車是空的
- 繼續購物
Izon Science Exoid TRPS 與傳統電動車表徵方法

Izon Science Exoid TRPS 與傳統電動車表徵方法
- 亞特蘭提斯生物科學公司
- 部落格
- 閱讀時間: 14 分鐘
細胞外囊泡(EV)、脂質體和脂質奈米顆粒(LNP)等奈米藥物對於推動醫學進步具有巨大潛力。近年來,EVs 因其在診斷、治療和藥物傳輸方面的潛力而受到了廣泛關注。這些由細胞分泌的奈米級囊泡攜帶蛋白質、脂質和核酸等生物活性分子,使其成為細胞間通訊和生物標記的理想候選者。由於其天然來源和向特定細胞運送貨物的能力,EVs 成為臨床領域很有前途的工具,特別是在癌症治療、再生醫學和疫苗輸送等領域。
儘管 EVs 具有巨大潛力,但將基於 EVs 的應用轉化為臨床實踐在很大程度上取決於其可靠的特性。為了開發安全有效的 EV 療法,研究人員必須準確地了解其特性,例如尺寸、表面電荷和分子組成。特性分析不僅對於理解其功能至關重要,而且對於滿足嚴格的監管要求也至關重要。
在以下章節中,我們將探討 EV 特性在釋放其臨床潛力方面所扮演的關鍵角色。我們將比較常見的技術,強調它們的優點和局限性,並介紹可調電阻脈衝感測(TRPS)作為一種正在重塑該領域的新興技術。最後,我們將介紹 Exoid,這是一種利用 TRPS 技術提供精確、可重複和全面的 EV 表徵的尖端儀器,為奈米粒子研究和臨床應用樹立了新的標竿。
3 電動車特性的關鍵屬性
為了推進 EV 的臨床應用,徹底評估影響其功能和治療潛力的特定關鍵品質屬性 (CQA) 至關重要。以下是必須評估的關鍵參數:
- 粒徑和粒徑分佈 (PSD)
EVs 由大小、組成和生物源特性各異的多種亞型組成。 EV 亞型的特徵很複雜。粒徑是電動車的關鍵屬性,直接影響其穩定性、生物分佈和生物活性。 EVs 的大小影響其逃避免疫清除、與目標細胞有效相互作用以及向特定組織運送治療物質的能力。例如,較小的EVs可能在血液中循環更長時間,從而增強其輸送潛力,而較大的EVs可能更容易被免疫系統識別和清除。
粒徑分佈 (PSD) 進一步反映了 EV 群體的均勻性,這對於實現一致的生物行為至關重要。較窄的 PSD 表示群體同質,這對於可重複性至關重要,並確保 EV 表現出可預測的相互作用和治療效果。相反,較寬的 PSD 可能會導致 EV 功能變化並降低臨床應用中的整體功效。
準確測量粒度和 PSD 對於生產過程中的品質控制和批次間一致性至關重要。此外,了解這些參數可以幫助研究人員優化 EV 配方以實現特定的治療目標,例如提高輸送效率或調整生物分佈。這些指標對於滿足監管標準也很重要,因為尺寸和分佈的變化會影響產品的安全性和功效。因此,粒度和 PSD 分析是基於 EV 的奈米藥物的開發、生產和臨床轉化的基礎步驟。
- 電動電位(表面電荷)
電動汽車電池的表面電荷(以zeta電位量化)對於其在生物系統內的穩定性和相互作用至關重要。絕對電位越高,表示粒子間的靜電排斥力越強,以最大限度地降低儲存或管理過程中聚集的風險。相反,絕對電位越低,表示排斥力越弱,增加了粒子聚集的可能性。
透過評估不同製備條件下的 Zeta 電位,研究人員可以優化 EV 配方以增強穩定性和功能性,例如改善細胞吸收和相互作用。此參數還可作為 EV 生產和淨化過程中有價值的品質控制指標,確保品質一致並最大限度地減少批次間差異。因此,測量 Zeta 電位是改進和標準化奈米醫學應用的 EV 配方的關鍵步驟
- EV 濃度
樣本中 EV 的濃度是影響其治療和診斷效果的關鍵參數。準確測量 EVs 濃度可確保生產批次間品質的一致性,這對於研究和臨床應用的可重複性至關重要。它也直接影響輸送到目標細胞的生物活性分子的數量,從而決定治療結果。
EVs濃度不僅反映了顆粒的數量,還顯示了樣品的品質和分離方法的效率。精確的濃度測量可確保分離過程有效且不含污染物,這對於 EV 製備的純度和功能性都至關重要。
在臨床和診斷應用中,維持正確的 EV 濃度對於實現預期效果和可靠結果至關重要。濃度不足會降低療效,而濃度過高可能會帶來安全風險。此外,濃度是一項關鍵的品質控制指標,可確保批次間的一致性和臨床使用的法規合規性。
透過精確表徵這些屬性,研究人員可以確保基於 EVs 的產品的品質和性能,為其成功融入臨床應用鋪平道路。
比較電動車表徵技術以進行品質控制
有多種技術可用於表徵電動車,每種技術都可以對其特性提供獨特的見解。這些方法可以根據其測量尺寸、形狀、表面電荷和濃度的能力進行大致分類,其中一些方法在特定參數方面表現出色,而另一些方法則提供更全面的分析。
奈米粒子追蹤分析
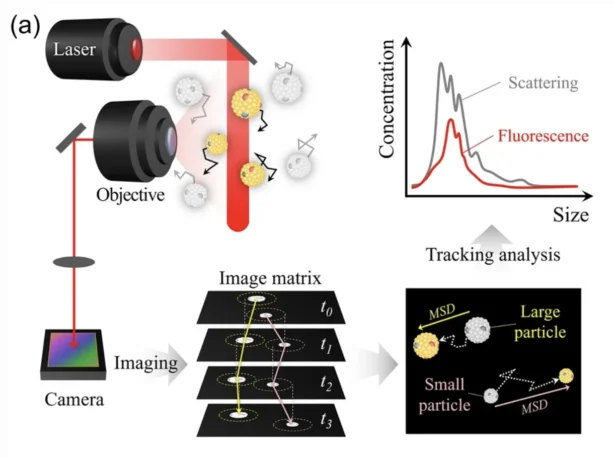
奈米粒子追蹤分析 (NTA) 是一種廣泛用於表徵 EV 的技術,可提供 PSD 和濃度的即時分析。 NTA 的工作原理是觀察懸浮液中的單一粒子,並在雷射照射下追蹤它們的布朗運動。透過分析運動來計算擴散常數,然後將其用於斯托克斯-愛因斯坦方程式來確定粒子的流體動力學直徑。 NTA 也考慮了溫度和黏度等環境因素,確保尺寸測量的準確性。
NTA 還可以與基於螢光的測量一起使用,使研究人員能夠檢查標記的 EV 亞群。粒子濃度是根據估計的照明量內追蹤的粒子數量來計算的,從而提供對 EV 豐度的定量見解。
儘管 NTA 具有諸多優勢,但它也有局限性。對於高濃度的樣品,它的準確度較低,需要仔細校準,並且動態範圍有限(10⁶–10⁹ 顆粒/毫升)。通常需要大量的樣品 (>250 µL),而且該技術僅限於低黏度樣品。此外,NTA 需要無振動環境以確保可靠的結果。
動態光散射
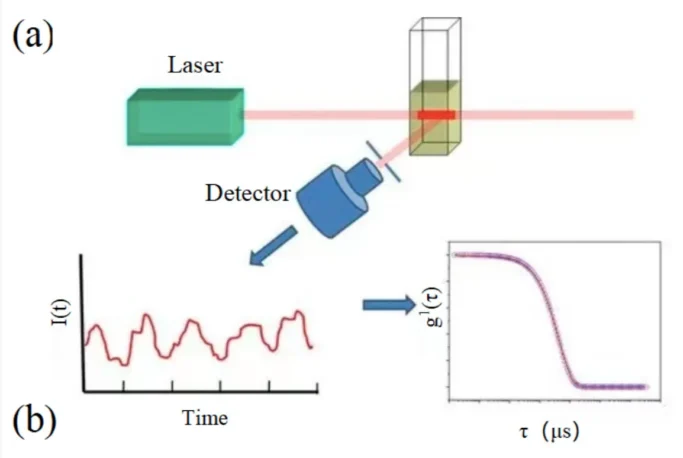
動態光散射 (DLS) 是另一種廣泛用於測量 EV 尺寸分佈的技術。透過分析由於粒子佈朗運動引起的光散射,DLS 可以估算懸浮液中 EV 的流體動力學直徑。它是一種自上而下的整合分析方法,可根據樣本中的波動訊號計算粒度。
雖然 DLS 可有效測定平均流體動力學直徑,但其靈敏度會隨著多分散群體而降低,並可能高估非球形 EV 的尺寸。 DLS 也難以檢測非常小或非常大的顆粒,而且由於它不是針對 EV 的,它可以檢測共分離的顆粒,例如脂蛋白和蛋白質聚集體,這可能會產生混淆的結果。
改進版本多角度動態光散射 (MADLS) 透過測量多個角度的散射解決了其中的一些限制。 MADLS 提供更精確的 PSD 和更高的分辨率,可以揭示在單一偵測角度下可能散射較弱的群體。
然而,DLS 和 MADLS 通常更適合直徑 1 nm 至 3 µm 的單分散樣品,但對於 150 nm 以下的顆粒有限制。對於精確的應用,例如電動車的表徵,準確了解光學特性(例如折射率)至關重要,因為這些特性會顯著影響結果。
奈米流式細胞儀
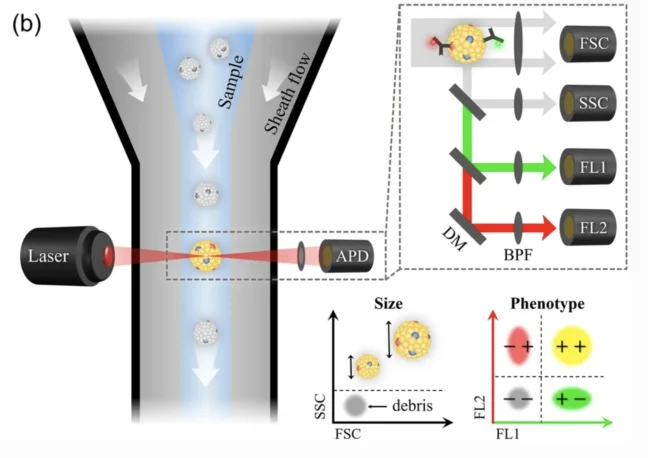
奈米流式細胞儀 (nFCM) 是一種特殊形式的流式細胞儀,專門用於分析直徑小於 1,000 奈米的奈米粒子(包括 EV)。 nFCM 能夠檢測小至 40 奈米的 EV,從而提供高解析度的單粒子分析。
在 nFCM 中,粒子以流體動力學的方式聚焦到微通道內的中心流中,並受到雷射激發。該技術使用單光子偵測器(SPCM)來測量光散射和螢光訊號。高分辨率側向散射光 (SSC) 提供有關顆粒大小和濃度的詳細信息,而螢光標記則能夠識別特定的亞群。
然而,nFCM 有其局限性。在高粒子濃度下,由於“群體效應”,可能會出現訊號重疊,導致巧合檢測並損害定量準確性。為了緩解這種情況,需要將樣品稀釋到最佳範圍(約 10⁷ 至 10⁹ 顆粒/毫升)。此外,用於螢光標記的兩親染料可以形成膠束或聚集體,從而可能產生背景訊號。因此,必須納入對照,例如僅染料或緩衝液樣品,以確保螢光標記和後續分析的可靠性。
可調電阻脈衝感測 (TRPS)
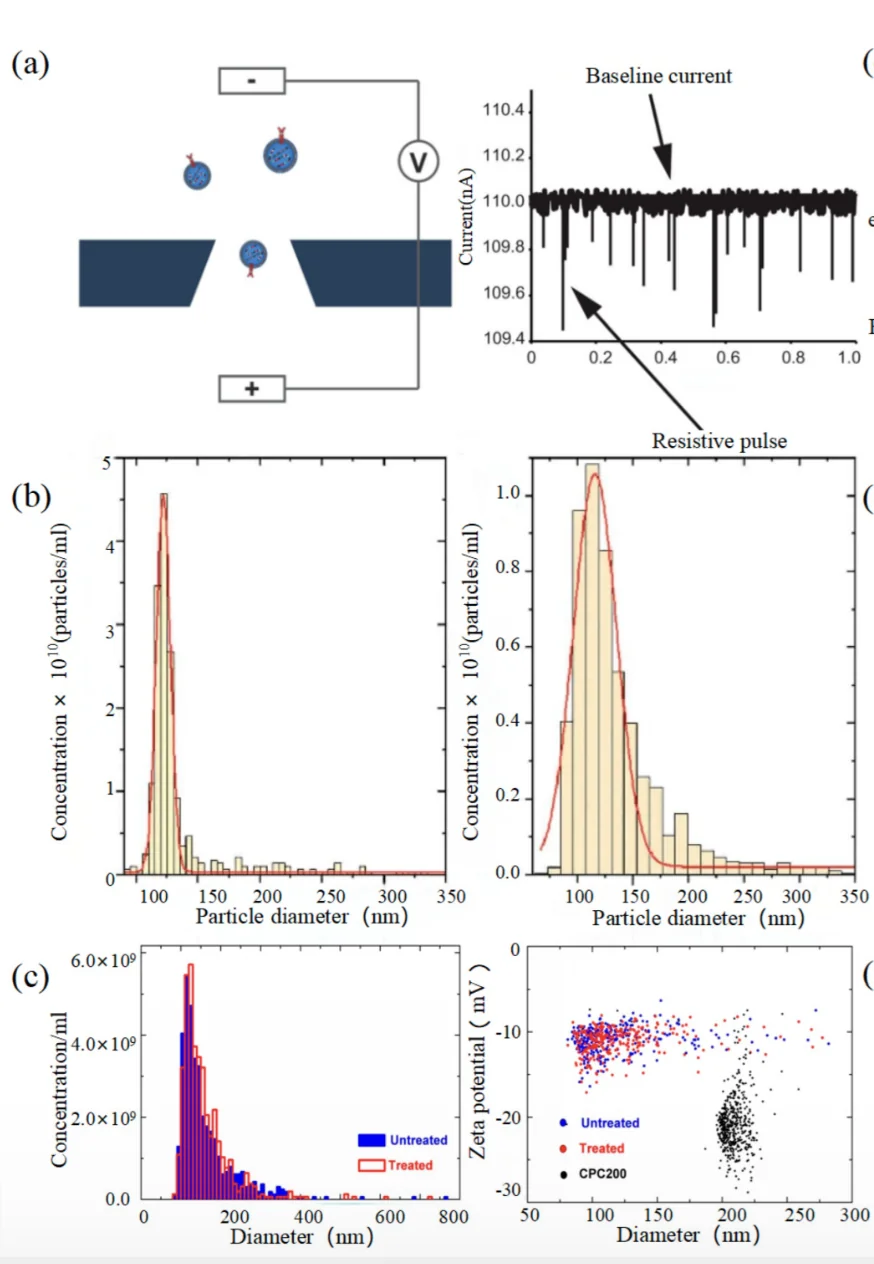
可調電阻脈衝感測 (TRPS) 是一種單粒子表徵技術,能夠高精度、高準確度地測量 PSD、濃度和 zeta 電位。與光學方法不同,TRPS 透過檢測粒子穿過奈米孔時阻抗的變化來以電力方式運作。當粒子穿過孔隙時,記錄下阻抗的變化,從而可以確定粒子的大小、濃度和表面電荷。
TRPS 採用一種裝置,該裝置由兩個腔室組成,腔室之間由奈米多孔膜隔開,兩側都有電極。膜上的電位差會產生電流,當電導率低的粒子穿過孔隙時,電阻會增加。這種電阻導致電流訊號明顯下降,由此可根據脈衝幅度和持續時間計算出粒子尺寸和電位。濃度測量是根據隨時間變化的電阻脈衝頻率得出的。
TRPS 的可調諧性,透過可調節的孔徑和多壓力校準,提高了其奈米顆粒分析的準確性。此功能可精確測量小至約 37 nm 的 EV,即使在多分散樣本中也是如此。此外,可以使用界面活性劑來防止顆粒聚集,進一步提高測量的可靠性。
與 NTA、DLS 和 nFCM 等基於光學的技術相比,TRPS 提供了卓越的尺寸分辨率,尤其是對於單模和多模樣本。它的取樣率更高,高達 500 kHz,超過了光學方法所需的毫秒級曝光時間,從而實現了更快、更動態的分析。此外,TRPS 可以分析更廣泛範圍內的粒子濃度,從 10⁵ 到 10¹⁴ 粒子/毫升,使其特別適合 EV 量化。雖然 TRPS 在準確度和動態範圍方面表現出色,但適當優化孔徑、電壓和樣品製備等變數對於獲得可靠的結果至關重要。
非對稱流場流分餾與多角度光散射耦合
非對稱流場流分餾與多角度光散射相結合(AF4-MALS)將基於尺寸的分離與線上檢測相結合以分析奈米顆粒。 AF4 透過平衡顆粒的布朗運動和開放、暢通的通道內的垂直流場,根據顆粒大小分離顆粒。由於擴散係數較快,較小顆粒會較早洗脫,而較大顆粒則會較晚洗脫。
與 MALS 結合,該方法可以提供高解析度的粒徑分佈以及質量和數量加權的粒子濃度,同時最大程度地減少樣品的相互作用或變形。
離心液體沉降
離心液體沉降法 (CLS) 根據旋轉盤中的沉澱時間來測量 PSD,旋轉盤中含有密度梯度,通常是蔗糖溶液。根據斯托克斯定律,粒子根據大小、密度和形狀的差異而被分離。基於光的檢測方法用於監測沉積物,尺寸校準通常依賴已知密度的粒子標準。雖然 CLS 不提供直接的數字加權濃度輸出,但它會產生基於強度的分佈,指示基於質量的濃度。準確的濃度測量可能需要額外了解粒子密度、光學特性以及與獨立濃度方法的比較。
電子顯微鏡
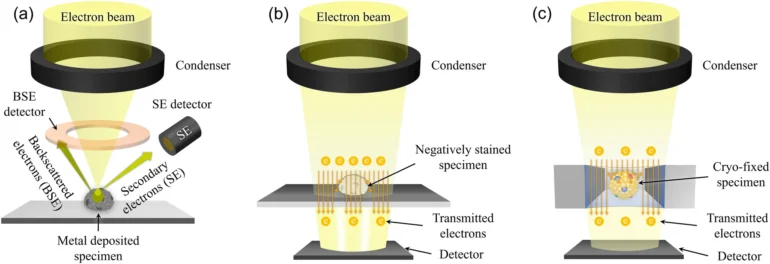
電子顯微鏡 (EM),包括透射電子顯微鏡 (TEM) 和掃描電子顯微鏡 (SEM),廣泛用於對包括電動車在內的奈米級樣品進行成像。 TEM 採用穿過樣品的電子束,適合檢查電動車的內部結構。相比之下,SEM 分析散射電子,提供詳細的表面結構資訊。這兩種技術都可以提供高達 1 奈米的分辨率。
儘管 EM 分辨率較高,但它也有局限性。 TEM 和 SEM 的樣品製備涉及固定和脫水,這可能會扭曲 EV 形態。 EVs 缺乏內部結構支撐,脫水後可能會塌陷成杯狀。為了解決這些問題,可以採用冷凍透射電鏡 (cryo-TEM)。透過將 EV 樣品嵌入液態氮溫度下的玻璃冰中,低溫透射電鏡 (cryo-TEM) 無需固定和脫水,保留了 EV 的天然形態。然而,挑戰仍然存在,例如手動選擇的成像區域可能存在感知偏差,以及難以估計整體人口特徵。
原子力顯微鏡
原子力顯微鏡(AFM)是一種捕捉奈米級樣品表面結構的強大技術。它透過使用與樣品表面相互作用的懸臂(探針)來操作。當探頭因表面形態變化而變形時,可以透過雷射反射到位置敏感光電二極體上來檢測變形。這使得 AFM 能夠產生表面拓撲的真實 3D 影像,使其成為表面結構分析的有價值的工具。
然而,EV 缺乏內部結構支撐,這可能導致樣品製備和成像過程中變形。為了提高成像質量,AFM 通常與單株抗體固定相結合,以穩定 EV,從而實現更準確的探針掃描。儘管存在這些挑戰,AFM 仍然是確定詳細表面拓撲結構的可靠方法。
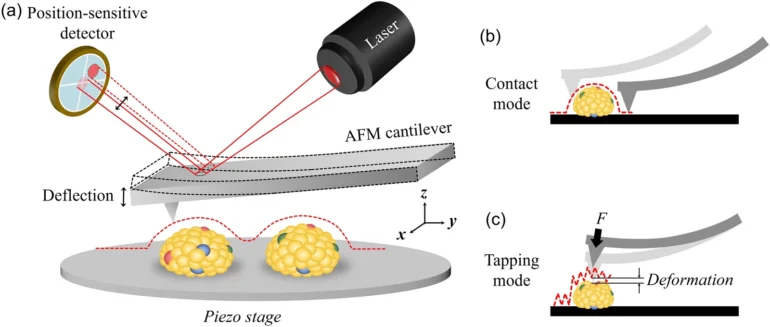
表1: 比較八種用於電動車表徵的正交方法。
| 單粒子分析 | 整合分析 | |||||||
| 類型 | 異戊二烯丙基氯化銨 | NTA | 流式細胞儀 | AFM | EM | AF4 移動輔助發射系統 | 華彩 | 移動性差速煞車系統 |
| 檢測類型 | 電流 | 光散射、螢光 | 光散射、螢光 | 燈光位置 | 散射/透射電子 | 光散射 | 光散射 | 光散射 |
| 檢測尺寸 | > 40 奈米 | > 50 奈米 | > 50 奈米 | > 1 奈米 | > 1–2奈米 | > 20奈米 | > 20奈米 | > 1 奈米 |
| 濃度 | 可以 | 可以 | 可以 | 沒有 | 沒有 | 是的,不是直接 | 是的,不是直接 | 是的,不是直接 |
| 尺寸 | 可以 | 可以 | 可以 | 可以 | 可以 | 可以 | 可以 | 可以 |
| 收費 | 可以 | 可以 | 沒有 | 沒有 | 沒有 | 沒有 | 沒有 | 可以 |
| 三方圈 | 沒有 | 沒有 | 沒有 | 可以 | 可以 | 沒有 | 沒有 | 沒有 |
TRPS – 可靠且精確的解決方案
每種奈米粒子表徵分析技術都有其限制。為了全面表徵 EV(包括 PSD、濃度和形態等參數),研究人員通常需要比較多種正交方法的結果。當處理在很寬尺寸範圍內呈現多分散分佈的複雜生物樣本時,這一點變得尤為重要。
在奈米粒子研究中,精確度和可靠性對於產生高品質的數據至關重要。選擇合適的分析技術至關重要,特別是對於多分散或複雜的樣品。雖然 DLS 和 NTA 等傳統方法被廣泛使用,但 TRPS 等先進技術已成為精確單粒子分析的強大工具。
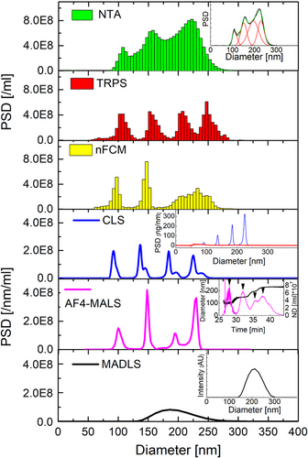
一項比較研究 Vogel 等人(2021) 凸顯了TRPS在克服複雜樣本挑戰的優勢。在使用 NIST 可追溯聚苯乙烯顆粒的雙峰混合物(1 和 1 nm 的比例為 100:200)測試中,MADLS 無法分辨不同的顆粒特徵,僅顯示出廣泛的分佈。對於三峰混合物(60、100 和 150 nm 粒子),TRPS 和 nFCM 提供了準確的分辨率,而 NTA 低估了最小粒子數量,報告值為 2-5%,而不是預期的 33.3%。四峰樣本揭示了其他技術的進一步限制。雖然 TRPS、CLS 和 AF4-MALS 實現了清晰的分辨率,但 TRPS 在多次運行中表現出了強烈的可重複性。儘管 nFCM 最初可以分辨四峰樣品,但是當對多次運行的數據進行平均時,分辨率會降低,從而合併 200 和 240 nm 粒子的峰值。
(CPN100/CPN150/CPN200/CPN240 at 25/25/25/25)
(CPN100/CPN150/CPN200/CPN240 at 10/50/30/10)
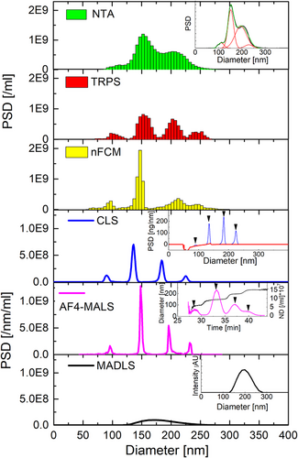
圖7: 四峰樣品的 NTA、TRPS、nFCM、CLS、AF4-MALS 和 MADLS 測量。 剩下: (CPN100/CPN150/CPN200/CPN240 at 25/25/25/25). 對: (CPN100/CPN150/CPN200/CPN240 為 10/50/30/10)。 NTA、TRPS、nFCM 和 MADLS 測量結果在 3 次運行中取平均值,而 CLS 測量結果在 2 次運行中取平均值。參考: https://doi.org/10.1002/jev2.12052
當分析透過尺寸排阻層析法製備的富含 EV 的血漿級分時,TRPS 再次表現出色,提供了可重複的尺寸和濃度測量,變異係數低於 10%。相較之下,NTA 始終高估濃度,而 nFCM 則低估較小顆粒的濃度。 AF4-MALS 雖然在某些情況下很精確,但由於難以針對非均勻生物樣本調整協議,因此難以量化 EV 濃度。
隨著奈米粒子研究在臨床和環境應用領域的進展,測量尺寸、濃度和表面電荷的可靠技術變得越來越重要。 Vogel 等人的比較研究。強調了 NTA 和 MADLS 等基於光學的方法的局限性,特別是對於多分散或複雜樣本。相較之下,TRPS 成為一種脫穎而出的方法,可在各種粒徑和樣品複雜程度下提供高解析度、可重複的結果。由於其能夠解析複雜的多分散樣本並提供高分辨率數據,因此 TRPS 成為 EV 特性分析中有價值的工具。
Exoid 簡介:使用 TRPS 進行高階奈米顆粒表徵
这 外星人 是 Izon 用於奈米粒子表徵的最先進的儀器,採用了 Izon 獨有的尖端技術 TRPS。雖然存在電阻脈衝感測 (RPS) 方法,但 Exoid 脫穎而出,成為唯一具有可調功能的系統,可在粒度、濃度和 zeta 電位測量方面實現無與倫比的精度。
TRPS 的工作原理是測量單個奈米粒子通過可調節的奈米孔時的情況。透過調整奈米孔的尺寸,使用者可以根據需要調整測量值以達到特定的尺寸範圍,從而確保獲得高解析度的數據。這種單粒子方法避免了集合技術中固有的偏差,其中較大的粒子會掩蓋較小群體的大小分佈。同時測量粒度和電位的能力對於了解複雜粒子分散體(例如外泌體、脂質奈米顆粒和病毒樣顆粒)的特性特別有價值。
Exoid 的主要特點
- 精確測量:
- Exoid 可以測量 40 nm 至 11 µm 範圍內顆粒的大小和濃度。
- 對於尺寸和電位測量,範圍是 40–2000 nm。
- 該系統提供對 PSD 的高解析度洞察,使其成為異質樣本的理想選擇。
- 校準和標準化:
- Exoid 採用 Izon 提供的以 NIST 可追溯顆粒為特徵的校正標準。
- 校準可確保一致且可重複的結果,並透過即時指標監測實驗期間的系統穩定性和訊號雜訊比。
- 跨應用程序的多功能性:
- Exoid 適用於分析各種奈米顆粒類型,包括 EV、脂質奈米顆粒、單株抗體製劑和病毒樣顆粒。
- 其廣泛的檢測範圍使其能夠適應多個學科和行業的研究。
- 友好的用戶界面:
- Exoid 提供自動化資料處理和乾淨、直覺的資料視覺化平台。
- 雖然 TRPS 需要一些技巧來優化電壓、壓力和奈米孔拉伸等參數,但這些努力會獲得精確可靠的數據。
TRPS – 細胞外囊泡表徵的黃金標準
準確的表徵對於推進 EV 在診斷和治療領域的應用至關重要。儘管 DLS 和 NTA 等傳統方法在處理複雜、多分散樣品時存在局限性,但 TRPS 卻可以透過精確的單粒子分析提供變革性的解決方案。 Exoid 採用 TRPS 提供動力,即使對於複雜的樣品,也能提供無與倫比的尺寸、濃度和 zeta 電位測量精度。其可調節的奈米孔技術、即時校準和適應性使其成為 EV 研究的寶貴工具,可確保滿足臨床和轉化應用需求的高解析度數據。
若要了解 Exoid 如何增強您的 EV 特性分析工作流程,請立即聯絡我們,採取下一步措施,以獲得精確可靠的結果!
參考
Kwon, Y., Park, J. 在單粒子層次分析細胞外囊泡的方法。 微納系統通訊 10,14(2022)。 https://doi.org/10.1186/s40486-022-00156-5
馬克斯,C.; Maurizi,L.; Borchard,G.; Jordan, O.自組裝聚合物-SPIONs奈米粒子的表徵挑戰:正交方法的優勢。 詮釋。 J. Mol。 科學。 2022, 2316124。 https://doi.org/10.3390/ijms232416124
Théry C、Witwer KW、Aikawa E、Alcaraz MJ 等。 al.,2018 年細胞外囊泡研究的基本資訊(MISEV2018):國際細胞外囊泡學會的立場聲明和 MISEV2014 指南的更新。 J 細胞外囊泡。 2018年23月7日;1(1535750):10.1080。 doi: 20013078.2018.1535750/XNUMX。
Vogel R、Savage J、Muzard J、Camera GD、Vella G、Law A、Marchioni M、Mehn D、Geiss O、Peacock B、Aubert D、Calzolai L、Caputo F、Prina-Mello A. 使用正交技術測量多模合成參考材料和細胞外囊泡的顆粒濃度:誰能應對挑戰? J 細胞外囊泡。 2021 年 10 月;3(12052):e10.1002。 doi: 2.12052/jevXNUMX。
Welsh JA、Goberdhan DCI、O'Driscoll L、Buzas EI 等。等、MISEV 聯盟; Théry C、Witwer KW。細胞外囊泡研究的最少資訊(MISEV2023):從基礎到高級方法。 J 細胞外囊泡。 2024 年 13 月;2(12404):e10.1002。 doi: 2.12404/jevXNUMX。
吳 S, 趙 Y, 張 Z, 左 C, 吳 H, 劉 Y. 外泌體表徵技術的進展及應用:從動態光散射到超解析度成像技術。 光子。 2024; 11(2):101。 https://doi.org/10.3390/photonics11020101
Zhao Z、Wijerathne H、Godwin AK 和 Soper SA。細胞外囊泡(EV)的分離和分析方法。 細胞外囊泡環狀核酸. 2021;2:80-103. http://dx.doi.org/10.20517/evcna.2021.07




