- 您的购物车是空的
- 继续购物

当新冠疫情席卷全球时,mRNA疫苗的出现彻底改变了局面,证明了现代科学能够以多快的速度应对紧急的病毒威胁。虽然疫情是催化剂,但它也为这项正在重新定义整个传染病预防领域的技术提供了一次巨大的“概念验证”。 速度, 适应性和 可扩展性 mRNA 平台使得安全有效的疫苗剂量得以在创纪录的时间内开发并在全球范围内部署——这在传统疫苗学中是以前不可想象的壮举。
除了SARS-CoV-2之外,mRNA技术还为应对各种新发和地方性传染病提供了一套高精度、灵活的工具。mRNA技术使研究人员能够根据新的病毒变种或全新的病原体快速更新疫苗序列,已成为全球应对疫情的基石。从季节性流感和呼吸道合胞病毒(RSV)到艾滋病毒(HIV)和寨卡病毒等复杂目标,这种变革性的力量正推动我们迈向医学的“即插即用”时代,在这个时代,应对疫情的速度可以与疾病本身的传播速度一样快。
mRNA疫苗的核心原理是将合成的信使RNA序列递送至宿主细胞。该序列编码来自特定病原体的一种或多种抗原。mRNA进入宿主细胞后,细胞核糖体将其翻译成抗原蛋白,并通过主要组织相容性复合体(MHC)分子呈递给宿主细胞。这种呈递过程会激活CD8⁺细胞毒性T细胞(负责清除感染细胞)和CD4⁺辅助性T细胞(负责协调免疫反应和激活B细胞)。这种协调的免疫应答会产生中和抗体和记忆B细胞,从而提供即时保护和长期免疫力。

从以下途径了解更多关于功能性mRNA的结构元件: 开始.
为了最大限度地提高疫苗对抗各种传染病威胁的功效,研究人员采用了多种优化技术:
为了进一步提高性能,出现了两种创新形式:
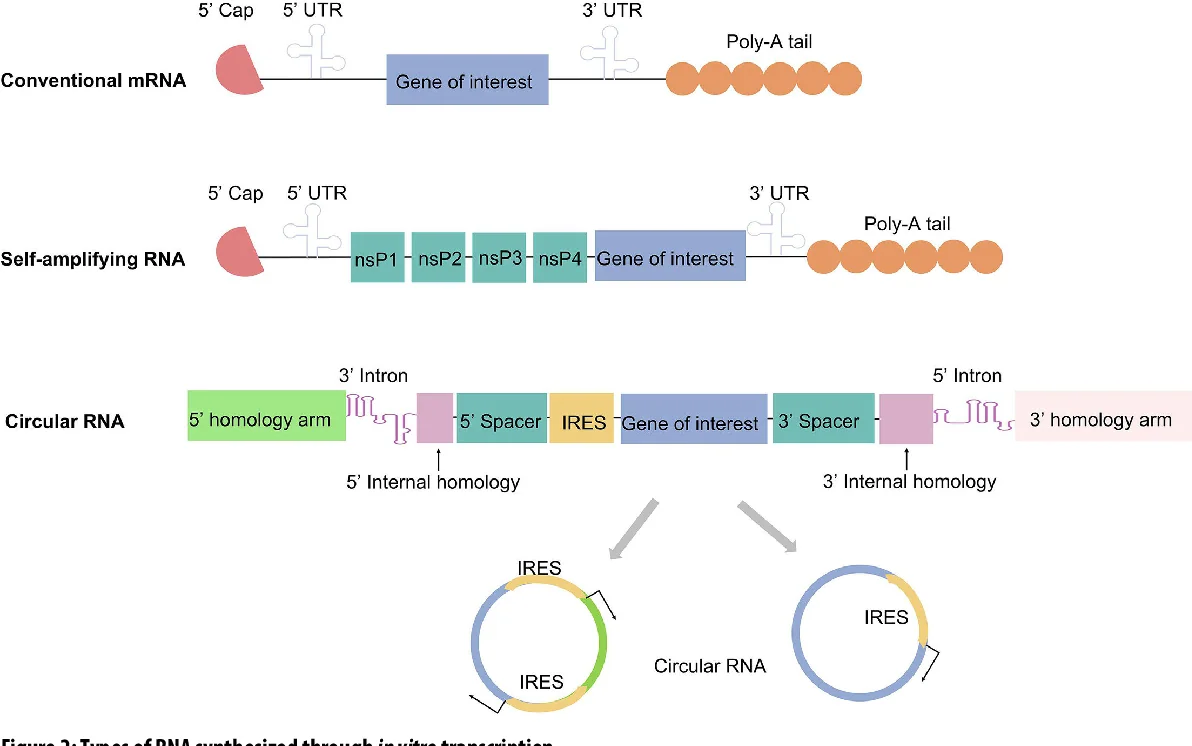
表1:常规mRNA、saRNA和circRNA的比较
| 特性 | mRNA | saRNA(自扩增RNA) | 环状RNA(circRNA) |
| 结构 | 线性RNA | 线性RNA + 病毒复制酶基因 | 共价闭合环状RNA |
| 长度 | 短(约1-5 kb) | 长(约 9–12 kb) | 可变,通常比 saRNA 短 |
| 细胞复制 | ❌否 | ✅ 是的(可自我放大) | ❌否 |
| 蛋白表达 | 中等程度,短暂 | 高(由于放大) | 持续、持久 |
| 所需剂量 | 中 | 低(由于自我复制) | 潜在低 |
| 稳定性 | 中等(易降解) | 适中(尺寸过大可能会影响稳定性) | 高(抗核酸外切酶) |
| 免疫原性 | 经过修改后进行控制 | 更高的先天免疫激活风险 | 先天免疫激活水平降低(新数据) |
| 制造复杂性 | 比较简单 | 更复杂(长链RNA,复制酶编码) | 复杂(需要环化步骤) |
| 交付(例如 LNP) | 完善的 | 由于尺寸原因,挑战更大。 | 仍在优化中 |
| 临床成熟度 | ✅ 最先进的(例如新冠疫苗) | ⚠ 早期临床阶段 | ⚠ 临床前/早期研究 |
| 主要优势 | 成熟、可扩展的平台 | 低剂量高效力 | 高稳定性及持久表达 |
| 关键限制 | 稳定性和冷链 | 尺寸大,潜在反应性 | 制造和翻译效率仍在不断发展 |
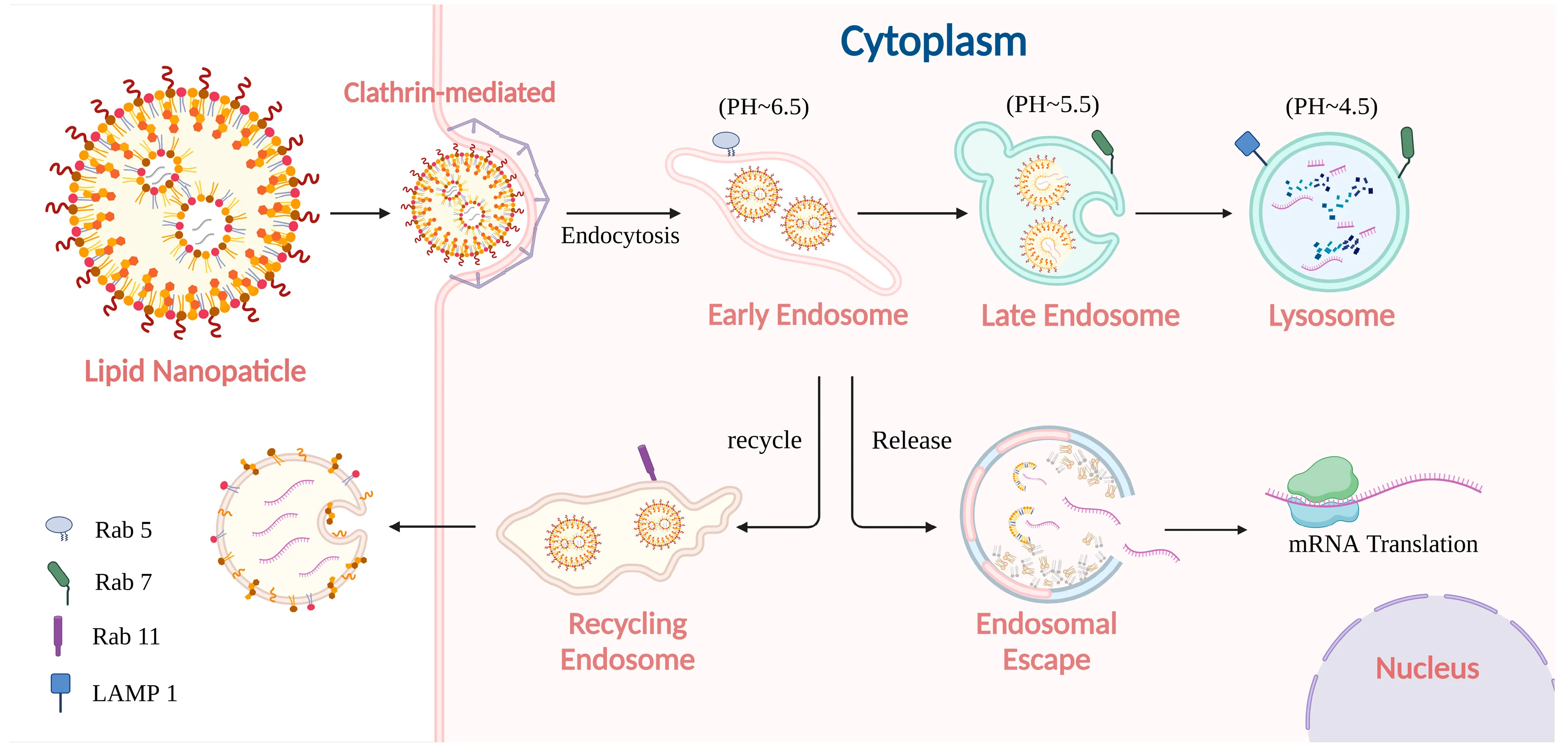
mRNA疗法面临的一项关键挑战是裸露RNA固有的不稳定性,它极易被生物环境中的核糖核酸酶(RNase)快速降解。此外,mRNA必须克服细胞膜屏障,因为其较大的体积和负电荷会阻碍其有效地被动进入细胞。
为了解决这些限制, 脂质纳米颗粒 (LNP) 脂质纳米颗粒(LNP)是mRNA疫苗的关键递送系统。这些疫苗的有效性与其LNP载体的理化性质密切相关。严格的表征不仅是质量控制步骤,更是确保疫苗性能稳定的基本要求。性质不明确的LNP会导致细胞摄取差异、免疫反应不可预测,并增加临床转化失败的风险。
脂质纳米颗粒 (LNP) 提供标准解决方案:
现代脂质纳米颗粒(LNP)是由可电离脂质、结构脂质、胆固醇和聚乙二醇化脂质组成的复杂结构。这些成分可以进行精确调控,以优化疫苗的生物分布和安全性。
*请查看我们关于“脂质纳米颗粒(LNP)制剂中的4种必需脂质“。
对于开发用于治疗传染病的 mRNA-LNP 制剂的研究人员来说,达到以下数值通常被认为是临床可行性的“黄金标准”:
运用 脉冲状研究人员可以高精度、单颗粒分辨率和快速周转来测量这些关键的 LNP 参数。
与在鸡蛋或细胞培养中生产的传统疫苗不同,mRNA疫苗采用无细胞技术。 体外转录(IVT) 流程。这种模块化设计使得我们能够对新出现的传染病做出如此迅速的反应。
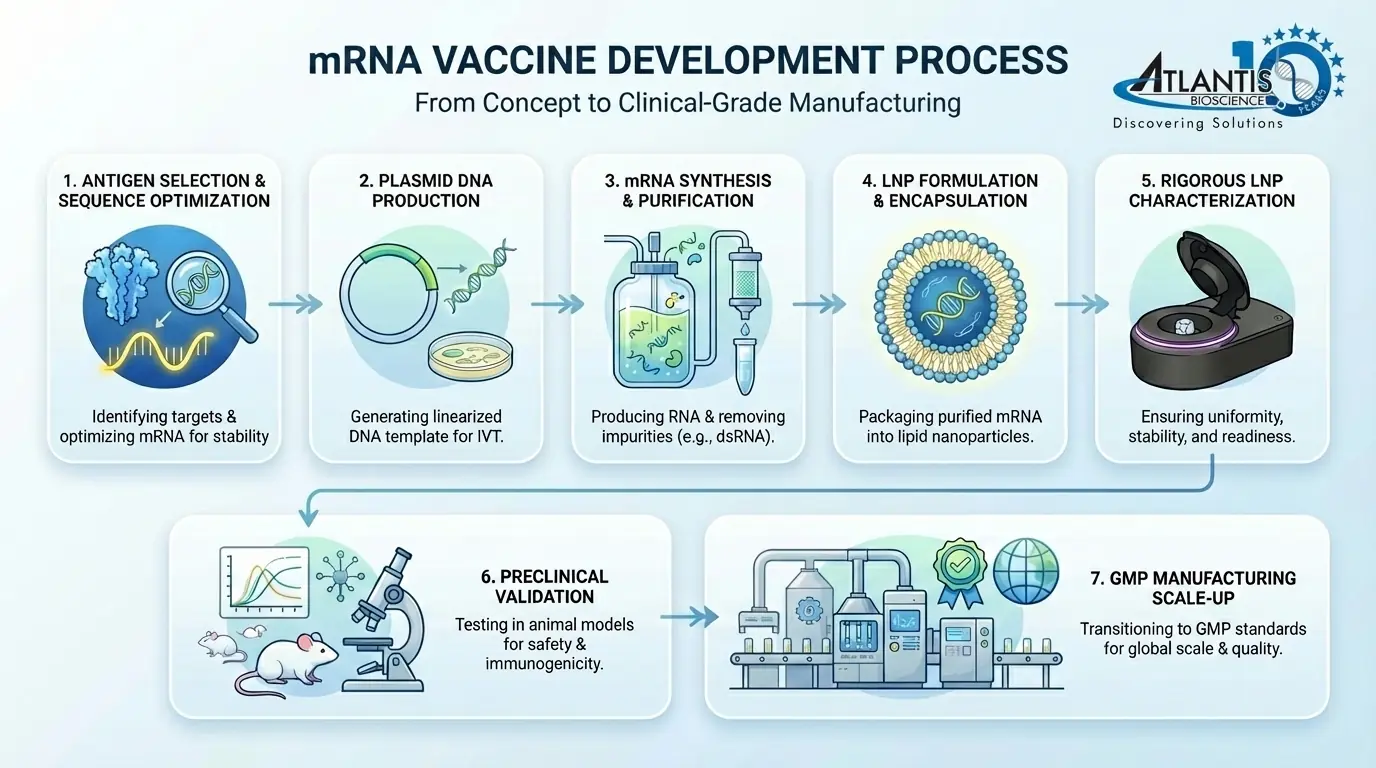
发展管道:
要点: 通过将高精度抗原设计与先进的 LNP 表征相结合,研究人员可以弥合发现与临床之间的差距,确保针对传染病的疫苗既安全又可重复。
辉瑞-BioNTech和Moderna新冠疫苗的成功仅仅是个开始。如今,mRNA平台正被用于对抗多种病原体,其中多个候选疫苗已进入后期临床试验阶段。
为什么mRNA是传染病控制的未来:
正在进行临床试验的选定mRNA疫苗候选药物(非COVID-19)
| 疾病/靶标 | 候选人/担保人 | NCT编号 | 状态和备注 |
| 流感(季节性) | mRNA-1010(摩德纳) | NCT05415462 | 第三阶段;已证实对 A 株具有阳性免疫原性;正在进行对 B 株的进一步测试。 |
| RSV | mRNA-1345(摩德纳) | NCT06067230 | 已获批准(mRESVIA);FDA 批准用于 60 岁以上成人;对下呼吸道疾病具有高效疗效。 |
| 寨卡病毒 | mRNA-1893(摩德纳) | NCT04917861 | 第二阶段;剂量确认研究,评估地方性流行地区的安全性/免疫原性。 |
| 巨细胞病毒(CMV) | mRNA-1647(摩德纳) | NCT05085366 | 第三阶段(CMVictory);在育龄妇女中进行评估;迄今为止最复杂的 mRNA-LNP(6 个序列),但 CMVictory 试验报告疗效欠佳,约为 6-23%,该项目正在终止。 |
尽管mRNA疫苗前景广阔,但仍面临若干关键的转化挑战,必须克服这些挑战才能充分发挥其对抗多种传染病的潜力。了解这些挑战对于疫苗研发者和整个疫苗生态系统中的利益相关者都至关重要。
1. mRNA的稳定性和完整性
mRNA本身非常脆弱,容易降解,因此需要精心设计、配制和处理。许多现有疫苗需要超低温储存,这给分发和获取带来了困难,尤其是在资源匮乏的地区。通过序列优化、修饰核苷酸或开发其他RNA形式(例如环状RNA)来提高mRNA的稳定性是目前的研究热点。
2. 配送效率和LNP优化
将mRNA高效递送至靶细胞对于实现稳健的抗原表达至关重要。脂质纳米颗粒(LNP)目前是主要的递送载体,但如何优化其组成、尺寸和靶向性以最大限度地提高摄取率、最大限度地减少脱靶效应并控制免疫激活仍然是一个挑战。
3. 批次间可重复性
一致性对于临床和监管方面的成功至关重要。mRNA合成、纯化或制剂方面的差异会影响抗原表达、免疫原性和安全性,因此批次间的可重复性是转化应用的一大障碍。
4. 从研究到GMP的规模化
虽然mRNA可以在小规模研究环境中快速合成,但要按照良好生产规范(GMP)标准进行规模化生产,则需要大量的基础设施、工艺优化和成本投入。在大规模生产中保持质量、纯度和效力并非易事,需要稳健的生产流程。
5. 监管和安全概况
疫情之外的长期安全性数据仍在不断涌现。新型mRNA平台的监管框架也在不断发展,要求开发人员全面解决安全性、免疫原性和批次间一致性问题。
mRNA疫苗的成功研发不仅仅需要精心设计的序列,更依赖于整合的工作流程、可靠的合作伙伴和强大的转化工具。应对诸如可重复性、可扩展生产和严格的脂质纳米颗粒(LNP)表征等挑战,需要疫苗研发管线多个阶段的协调配合。
合作伙伴喜欢 派克基因 为……提供基本服务 质粒 脱氧核糖核酸, mRNA 以及 mRNA/LNP 的产生使研究人员能够:
该整合解决了 mRNA 疫苗开发中常见的流程缺陷,确保从模板设计到封装的每一步都符合可重复和可扩展研究所需的标准。
对于mRNA疫苗的成功研发而言,稳健的分析方法、可重复性和可扩展的系统至关重要,尤其是在测量和表征脂质纳米颗粒(LNP)时。然而,诸如动态光散射(DLS)等传统技术提供的测量结果仅代表样本的平均值,这可能会掩盖LNP制剂内部的潜在异质性。例如,平均粒径为90 nm可能掩盖了少量粒径约为300 nm的较大聚集体,而这些聚集体可能会影响疫苗安全性并引发意外的免疫反应。
为了克服这一局限性,先进的单颗粒LNP表征技术变得越来越重要。诸如以下平台: 脉冲状, 基于 纳米孔脉冲传感(NPS)单独测量纳米颗粒,提供关于颗粒大小、浓度、zeta 电位和群体异质性的高分辨率信息。

Pulsoid 通过以下方式支持精确的 LNP 测量和 mRNA 疫苗开发工作流程:
这些工具共同构成了一个协同生态系统,可以应对传染病研究中的分析和生产挑战,增强对实验结果和转化工作流程的信心。
在亚洲, 亚特兰蒂斯生物科学 在连接mRNA开发生态系统中发挥着关键作用。通过将PackGene的生产能力与Pulsoid的先进表征技术相结合,我们为研究人员提供从质粒和mRNA合成到LNP制剂和临床前小鼠模型研究的全流程支持。 十年支持科学发现Atlantis Bioscience 构建了一个区域生态系统,将研究人员、临床医生和兽医合作伙伴联系起来,以促进转化研究并实现从实验室到临床的转化。这种整合方法加快了疫苗开发进程,并强化了从发现到临床应用的路径,从而提高了整个研发流程的可重复性、可扩展性和科学严谨性。
观看下方这段 YouTube 视频,了解更多关于 mRNA-LNP 疫苗平台的信息。
mRNA疫苗从根本上改变了我们对抗传染病的方式。其模块化特性和快速生产速度使其成为现代疫苗学的终极工具。随着我们不断改进脂质纳米颗粒(LNP)递送技术和提升表征标准,mRNA无疑将成为全球卫生安全的基础技术。
Aleem MT、Munir F、Shakoor A、Gao F。针对传染病的 mRNA 疫苗和未来方向。国际免疫药理学。 2024 年 6 月 30 日;135:112320。 doi:10.1016/j.intimp.2024.112320。
Danaei M、Dehghankhold M、Ataei S、Hasanzadeh Davarani F、Javanmard R、Dokhani A、Khorasani S、Mozafari MR. 粒径和多分散指数对脂质纳米载体系统临床应用的影响。Pharmaceutics. 2018 年 5 月 18 日;10(2):57。doi: 10.3390/pharmaceutics10020057。
Li S, Zheng L, Zhong J, Gao X. 推进传染病mRNA疫苗:关键组成部分、创新和临床进展。Essays Biochem. 2025年5月1日;69(2):EBC20253009。doi: 10.1042/EBC20253009。
Rezk N, McClean S. 利用 mRNA 疫苗对抗传染病的潜力。微生物生物技术。2025 年 8 月;18(8):e70212。doi: 10.1111/1751-7915.70212。
Schoenmaker L、Witzigmann D、Kulkarni JA、Verbeke R、Kersten G、Jiskoot W、Crommelin DJA。 mRNA-脂质纳米颗粒 COVID-19 疫苗:结构和稳定性。国际医药杂志。 2021 年 5 月 15 日;601:120586。 DOI:10.1016/j.ijpharm.2021.120586。
Wang J, Chen R, Xie Y, Qin X, Zhou Y, Xu C. 内吞/溶酶体逃逸脂质纳米颗粒平台增强癌症治疗中mRNA递送。Pharmaceutics. 2025年6月20日;17(7):803. doi: 10.3390/pharmaceutics17070803.

探索塑造 2026 年生物技术发展的十大趋势,从体内编辑和 RNA 疗法到空间组学和再生医学创新。