- 您的购物车是空的
- 继续购物

在不断发展的生物医学研究领域,创新工具在揭示癌症等复杂疾病的新见解方面发挥着关键作用。在这些工具中,细胞染色已成为不可或缺的工具,使科学家能够以前所未有的清晰度和精度观察和探究细胞过程。
加入我们,一起踏上探索癌症研究最新进展的旅程,这些进展由细胞染色的独创性推动。在这里,我们选择了五篇最近的出版物,展示了这些染色对阐明关键分子机制、确定新的治疗靶点和推动个性化医疗进步的变革性影响。
Zhang 等人开发了一种基于双特异性单链可变片段 (scFv) 的纳米接合器,旨在通过特异性靶向肿瘤细胞来增强巨噬细胞的吞噬活性。通过对细胞膜进行基因工程,作者获得了双特异性 scFv,包括抗 CD40 scFv(靶向巨噬细胞)和抗 CLDN18.2 scFv(靶向肿瘤细胞)。随后使用这些 scFv 涂覆 PLGA 核心,从而得到同时呈现抗 CD40 scFv 和抗 CLDN18.2 scFv 的纳米接合器。这些纳米接合器显著增强了免疫反应,包括增强巨噬细胞对肿瘤细胞的识别和吞噬作用、增强活化和抗原呈递以及提高细胞毒性 T 淋巴细胞活性。这些综合优势提高了对高度侵袭性的“冷”胰腺癌的抗肿瘤功效。总之,本研究提出了一种用于免疫治疗的多功能纳米接合器设计,通过基因工程整合抗体锚定膜来实现。
做过 和 二氧化O均为亲脂性碳菁染料,用作亲脂性示踪剂,对表达抗 CD40 scFv 和抗 CLDN18.2 scFv 的 KPC 细胞膜进行染色,以制备纳米接合体。它们还用于共培养实验,用于吞噬作用测定。此外, 迪瑞克 (见下图)用于标记近红外纳米接合体 体内 用于肿瘤靶向和生物分布分析以及抗肿瘤功效研究的成像。
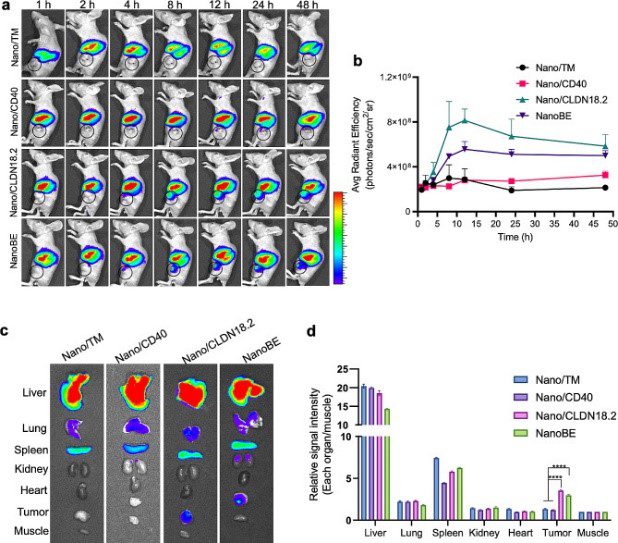
图 3 部分来自 Zhang et al. 肿瘤靶向和生物分布。 (A) 代表 体内 静脉注射 DiR 标记的 Nano/TM(KPC 细胞系膜)、DiR 标记的 Nano/CD40、DiR 标记的 Nano/CLDN18.2 和 DiR 标记的 NanoBE(表达抗 CD40 scFv 和抗 CLDN18.2 scFv 的纳米接合体)后,在指定时间点进行生物分布荧光成像。肿瘤用黑色圆圈表示。 (B) 在指定时间点施用粒子后肿瘤的平均信号强度。
来源:Zhang, Y., Li, Y., et.al., doi: 10.1186/s12951-024-02369-9
转载下 知识共享许可
在这项研究中,Prajapati 等人将富含亮氨酸的纤连蛋白跨膜蛋白 3 (FLRT3)(一种轴突引导分子 (AGM))确定为抑制 T 细胞活性的配体。这种抑制是通过非配位 5 (UNC5B) 实现的,UNC3B 是一种在激活的人类 T 细胞上上调的轴突引导受体。人源化斑马鱼模型用于研究 FLRT5-UNC5B 轴在 T 细胞抗肿瘤免疫和肿瘤浸润中的作用。这些模型分别用卵巢癌 (OVCAR-3) 或横纹肌肉瘤 (RD) 细胞系和 EpCAM 嵌合抗原受体 (CAR-T) 细胞或表皮生长因子受体 (EGFR)/CD405 双特异性 T 细胞接合器 (BiTE) 建立。肿瘤细胞用 mCherry 稳定表达以评估肿瘤生长,然后腹膜内注射用 ViaFluor 3 SE 染料标记的 T 细胞。作者证明,肿瘤上的 FLRTXNUMX 表达显著降低了 T 细胞介导的抗肿瘤免疫力,抑制了 T 细胞肿瘤环境 (TME) 募集/浸润,并减少了 T 细胞与肿瘤细胞的接触。这项研究提供了轴突引导蛋白模拟 T 细胞检查点的证据,肯定了它们作为癌症免疫治疗靶点的潜力。
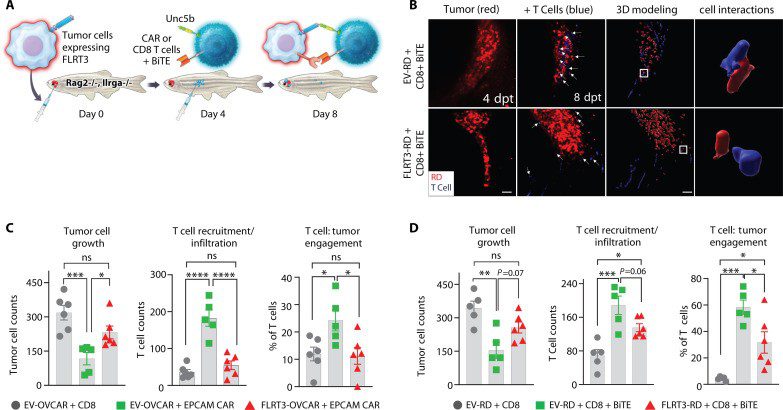
图 5 来自 Prajapati et al. FLRT3 抑制斑马鱼模型中的 T 细胞免疫、浸润和肿瘤参与。 (A) 代表性人源化斑马鱼模型示意图。 (B) 代表性显微镜图像显示 T 细胞 (蓝色) 与 RD 肿瘤细胞 (红色) 的募集 (左侧两幅图) 和紧密细胞相互作用 (参与) (右侧图)。3D 建模用于评估 T 细胞:肿瘤细胞参与。 (C) OVCAR-5 细胞与对照 CD8+ T 细胞、EV–OVCAR-5 + EpCAM CAR-T 细胞和 FLRT3–OVCAR-5 + EpCAM CAR-T 细胞对肿瘤生长、T 细胞募集/浸润和 T 细胞参与的影响。 (D) 与...一样 (C) 除了使用具有 EV-RD + EGFR-CD3 BiTE 或 FLRT3-RD + EGFR-CD3 BiTE 的 RD 肿瘤模型。
来源:Prajapati, K., Yan, C., et.al., doi: 10.1126/sciadv.adj4698
转载下 知识共享许可
与普遍认为额外的着丝粒本身会促进肿瘤生长的观点相反, 棕色 等。 人。,证明它们实际上会诱导由 DNA 损伤引发的线粒体凋亡。该过程由 Polo 样激酶 4 (PLK4) 促进,它会激活 PIDDosome。该研究利用 NucView® 530 Caspase-3 酶底物来量化活细胞中的细胞死亡。附图说明,过表达 Plk4 的细胞表现出 caspase-3 报告基因的激活增加,从转基因诱导后约 30 小时开始。数据还显示,这种细胞死亡是 PIDDosome 依赖性的;PIDDosome 的失活(通过丢失单个 PIDDosome 成分 - Caspase-2、Raidd 或 Pidd1)可以在 Plk4 mRNA 过表达的情况下减少死细胞的数量。这表明 Plk4 过表达响应额外的着丝粒而使 PIDDosome 参与启动细胞死亡。总之,这些发现揭示了着丝粒扩增的新的肿瘤抑制作用,表明在癌症治疗中具有潜在的治疗应用。
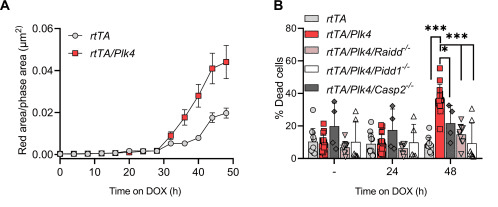
图 6 的一部分来自 Bruan et al. 着丝粒扩增导致PIDDosome依赖性的细胞死亡。 (A) 通过 IncuCyte 分析 (红色荧光面积/相面积,单位为 μm3) 测量了强力霉素治疗后多能造血祖细胞 (MPP) 中时间依赖性的 caspase-2 底物处理情况。 (B) 暴露于强力霉素 24 或 48 小时后,对 DAPI 和 Annexin V 阳性 MPP 细胞进行量化。
图片来源:Braun, V.、Karbon, G., 等., DOI: 10.1126/sciadv.adk0564
转载下 知识共享许可
研究由 卡尔班诺娃 et al. 发现黑色素瘤细胞释放含有 CD133 干细胞标记物的细胞外囊泡 (EV)。这些大型 EV 在黑色素瘤细胞分裂或迁移过程中观察到,富含脂滴和线粒体。这些 EV 作为能量燃料的储存器,可能在促进癌细胞扩散、迁移和最终支持癌症生长方面发挥作用。
该研究利用了 FEMX-I 细胞,这是一种高度侵袭性的黑色素瘤细胞系。研究人员能够通过采用各种实验技术对细胞进行染色来确定细胞外囊泡 (EV) 上脂质滴和线粒体是否同时存在。这些技术包括使用不同的荧光染料组合来标记脂质滴(LipidSpot™ 610、BODIPY™ 493/503)或线粒体(MitoTracker™ Red CMXRos、 MitoView™ Fix 640),以及 60 kDa 线粒体抗原或脂滴相关脂肪细胞因子的免疫标记(在用 COX8-mCherry 转染的细胞中)。细胞还与 荧光偶联WGA 突出细胞膜上的糖复合物。
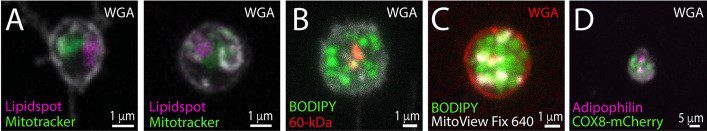
Karbanova 的“图 8”部分 et al. FEMX-I 细胞与 (A) MitoTracker™ Red CMXRos 或 (C) MitoView™ Fix 640,并与荧光染料共染色 (A) LipidSpot™ 610 或 (C) BODIPY™ 493/503,或 (B) 用抗 60 kDa 线粒体抗原抗体进行免疫标记,并用 BODIPY™ 493/503 染色。 (D) 或者,用抗脂肪素抗体对 COX-8-mCherry 转染的 FEMX-I 细胞进行免疫标记。样品还与荧光结合的 WGA 共染色,以突出显示细胞膜上的糖复合物。
图片来源:Karbanova,J.,Deniz,IA., 等., DOI: 10.1186/s12964-024-01471-7
转载下 知识共享许可
在这项研究中, 肖汉 等. 确定了 Moloney 鼠白血病病毒 1 (PIM1) 激酶的前病毒整合位点是脂质滴 (LD) 积累的驱动因素。他们证明了这一事件在营养应激期间前列腺癌细胞增殖和存活中起着关键作用。作者表明,PIM1 通过一种新的信号传导轴 (GSK3β-PPARα) 起作用,包括直接磷酸化和抑制 GSK3β,随后激活 PPARα 以促进 LD 积累。 LipidSpot488 和 脂质斑点610 用于评估 细胞/组织 研究。
作者还进一步证明,使用基因或化学方法靶向 PIM1 或 PPARα 信号传导可消除前列腺癌中 LD 积累和 PIM1 诱导相关的增殖和存活优势。因此,靶向 PIM1 和/或阻断 LD 利用可能代表一种有前途的前列腺癌治疗策略。
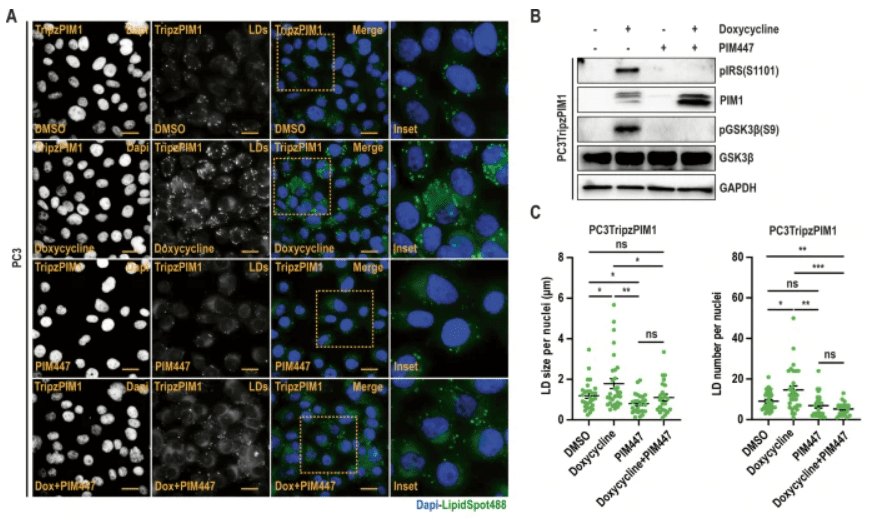
Chauhan 等人的图 2 的一部分 (A) 仅用强力霉素治疗和与 PIM 抑制联合治疗后,PC3TripzPIM1 细胞(稳定表达强力霉素诱导的 PIM1 载体的前列腺癌细胞系)中的 LD 代表性图像。 (B) 仅用强力霉素治疗和与 PIM 抑制联合治疗后,对 PC3Tripz-PIM1 细胞进行蛋白质印迹分析。 (C) 量化每个细胞核的 LD 大小和数量(n > 30 个细胞/组)。
图片来源:Chauhan, S., Casilla, AL., et.al., doi: 10.1038/s41388-023-02914-0
转载下 知识共享许可
这些特色出版物中介绍的染料来自 Biotium。作为尖端染料和染色剂的领先开发商,Biotium 站在这场革命的前沿,为研究人员提供各种高品质试剂,以满足现代实验范式的需求。凭借对卓越和创新的承诺,Biotium 的染料使科学家能够自信而高效地探索细胞生物学的复杂性。
案例
Braun VZ、Karbon G、Schuler F、Schapfl MA、Weiss JG、Petermann PY、Spierings DCJ、Tijhuis AE、Foijer F、Labi V、Villunger A。额外的着丝粒会延迟 DNA 损伤驱动的肿瘤发生。Sci Adv。2024 年 29 月 10 日;13(0564):eadk10.1126。doi: 0564/sciadv.adk2024。电子版 29 年 38552015 月 10980279 日。PMID:XNUMX;PMCID:PMCXNUMX。
Chauhan SS、Casillas AL、Vizzerra AD、Liou H、Clements AN、Flores CE、Prevost CT、Kashatus DF、Snider AJ、Snider JM、Warfel NA。PIM1 驱动脂质滴积聚,促进前列腺癌的增殖和存活。Oncogene。2024 年 43 月;6(406):419-10.1038。doi:41388/s023-02914-0-2023。14 年 XNUMX 月 XNUMX 日电子版。
Karbanová J、Deniz IA、Wilsch-Bräuninger M、de Sousa Couto RA、Fargeas CA、Santos MF、Lorico A、Corbeil D。黑色素瘤细胞分裂过程中会释放含有脂质滴和线粒体的细胞外脂质体。Cell Commun Signal。2024 年 19 月 22 日;1(57):10.1186。doi:12964/s024-01471-7-XNUMX。
Prajapati K、Yan C、Yang Q、Arbitman S、Fitzgerald DP、Sharee S、Shaik J、Bosiacki J、Myers K、Paucarmayta A、Johnson DM、O'Neill T、Kundu S、Cusumano Z、Langermann S、Langenau DM、Patel S、Flies DB。FLRT3-UNC5B 检查点通路可抑制基于 T 细胞的癌症免疫疗法。Sci Adv. 2024 年 10 月;9(4698):eadj10.1126。doi: 4698/sciadv.adj2024。电子版 1 年 XNUMX 月 XNUMX 日。
Zhang H, Li Y, Kang H, Lan J, Hou L, Chen Z, Li F, Liu Y, Zhao J, Li N, Wan Y, Zhu Y, Zhao Z, Zhang H, Zhuang J, Huang X. 基因工程膜基纳米接合器用于胰腺癌免疫治疗。纳米生物技术杂志。2024 年 11 月 22 日;1(104):10.1186。doi:12951/s024-02369-9-XNUMX。


了解当前使用间充质干细胞 (MSC) 进行癌症治疗的临床试验。了解如何研究间充质干细胞来治疗癌症并减轻传统疗法的副作用。