การบำบัดด้วยภูมิคุ้มกันมะเร็งมีความก้าวหน้าอย่างมากในช่วงไม่กี่ปีที่ผ่านมา ด้วยการเกิดขึ้นของแนวทางใหม่ๆ เช่น การบำบัดด้วยทีเซลล์ด้วยไคเมอริกแอนติเจนรีเซพเตอร์ (CAR) และการบำบัดด้วยทีเซลล์ด้วยทีเซลล์รีเซพเตอร์ (TCR) กลยุทธ์ทั้งสองเกี่ยวข้องกับการควบคุมพลังของระบบภูมิคุ้มกันเพื่อต่อสู้กับมะเร็ง แต่มีความแตกต่างที่สำคัญบางประการระหว่างทั้งสองวิธี
In การบำบัดด้วย T-cell ของรถยนต์ , ทีเซลล์ถูกนำมาจากเลือดของผู้ป่วย, ดัดแปลงพันธุกรรมเพื่อผลิตไคเมอริกแอนติเจนรีเซพเตอร์, และจากนั้นเซลล์ CAR T-เซลล์ที่เป็นผลลัพธ์จะถูกส่งกลับไปยังผู้ป่วย CAR ช่วยให้ทีเซลล์จดจำแอนติเจนของเซลล์มะเร็งที่จำเพาะและกระตุ้นทีเซลล์ให้ฆ่าเซลล์มะเร็งเหล่านี้
การบำบัดด้วย TCR-T ทำงานคล้ายกับการบำบัดด้วยเซลล์ T-cell ของ CAR แต่แทนที่จะใช้ตัวรับแอนติเจน chimeric การบำบัดด้วย TCR จะดัดแปลงเซลล์ T ของผู้ป่วยเพื่อแสดง T-cell receptor (TCR) ที่จดจำแอนติเจนที่จำเพาะบนเซลล์มะเร็ง เมื่อ T-cells ที่ได้รับการดัดแปลงถูกใส่กลับเข้าไปในตัวผู้ป่วยแล้ว พวกเขายังสามารถค้นหาและทำลายเซลล์มะเร็งที่แสดงแอนติเจนที่เป็นเป้าหมายได้
ความแตกต่างระหว่าง CAR T-Cell Therapy และ TCR-T Therapy
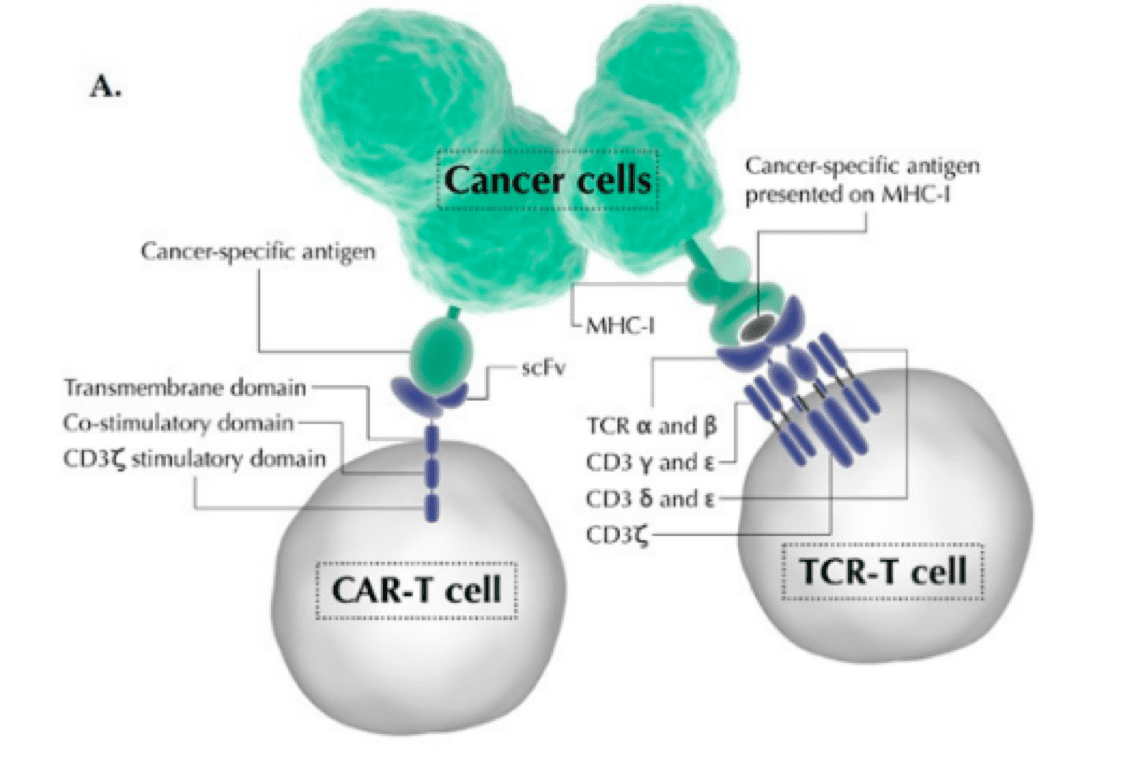
โครงสร้าง T-เซลล์ CAR และ T-เซลล์ที่ออกแบบโดย TCR นั้นแตกต่างกัน CAR-T โครงสร้างเซลล์ ประกอบด้วยโดเมนภายในเซลล์และนอกเซลล์ที่ได้รับการออกแบบทางวิศวกรรม โดเมนนอกเซลล์ประกอบด้วยชิ้นส่วนที่แปรผันได้สายเดี่ยว (ซึ่งประกอบด้วยโดเมนการจับแอนติเจนของแอนติบอดี) เพื่อจดจำแอนติเจนที่จำเพาะบนพื้นผิวของเซลล์เพื่อกระตุ้นการส่งสัญญาณภายในเซลล์ที่นำไปสู่การกระตุ้นทีเซลล์ การบำรุงรักษาการเปิดใช้งาน T-cell และการอยู่รอดของ CAR T-cell นั้นได้รับการปรับปรุงเพิ่มเติมโดยการเพิ่มโดเมน costimulatory ให้กับส่วนภายในเซลล์ของ CAR T-cell
ในทางกลับกัน ทีเซลล์ที่ออกแบบโดย TCR ใช้ตัวรับ TCR ที่เกิดขึ้นตามธรรมชาติ (หรือดัดแปลงน้อยที่สุด) เพื่อจดจำแอนติเจนของเนื้องอกที่นำเสนอโดยโมเลกุลสารเชิงซ้อนที่เข้ากันได้ของฮิสโตคอมแพทิตีที่สำคัญ (MHC) ความแตกต่างที่สำคัญอื่น ๆ คือเป้าหมาย CAR T-cells รู้จักเฉพาะแอนติเจนบนผิวเซลล์มะเร็งเท่านั้น และโดยทั่วไปแล้วแอนติเจนบนผิวเหล่านี้จะไม่แสดงออกบนเนื้องอกที่เป็นของแข็ง ในทางตรงกันข้าม ทีเซลล์ที่ออกแบบโดย TCR ไม่เพียงแต่กำหนดเป้าหมายแอนติเจนที่พื้นผิวเท่านั้น แต่ยังกำหนดเป้าหมายภายในเซลล์ด้วย ดังนั้น การบำบัดด้วย TCR จึงนำไปใช้ได้กว้างกว่า เนื่องจากมีลำดับที่จำเพาะต่อเนื้องอกภายในเซลล์และนำเสนอใน MHC มากกว่ามีโปรตีนที่จำเพาะต่อเนื้องอกบนพื้นผิว
แผนผังของผลิตภัณฑ์ภูมิคุ้มกันบำบัดเซลล์ CAR-T และ TCR-T ทั่วไป เครดิต: Ivica, NA; Young, CM doi.org/10.3390/healthcare9081062 ผลิตซ้ำภายใต้ สัญญาอนุญาตครีเอทีฟคอมมอนส์
ภาพรวมโดยย่อของ CAR T-Cell Therapy
การบำบัดด้วยเซลล์ T-CAR ได้รับการพัฒนาและบุกเบิกเพื่อรักษามะเร็งเม็ดเลือด โดยเฉพาะมะเร็งเซลล์ B เช่น มะเร็งเม็ดเลือดขาวชนิดเฉียบพลันชนิดลิมโฟบลาสติก (ALL) และมะเร็งต่อมน้ำเหลืองชนิดนอนฮอดจ์กิน มะเร็งประเภทนี้มักจะรักษาได้ยากด้วยเคมีบำบัดแบบดั้งเดิมและการฉายแสง และการบำบัดด้วยเซลล์ CAR T-cell ได้แสดงให้เห็นผลลัพธ์ที่น่ายินดีในการทดลองทางคลินิก
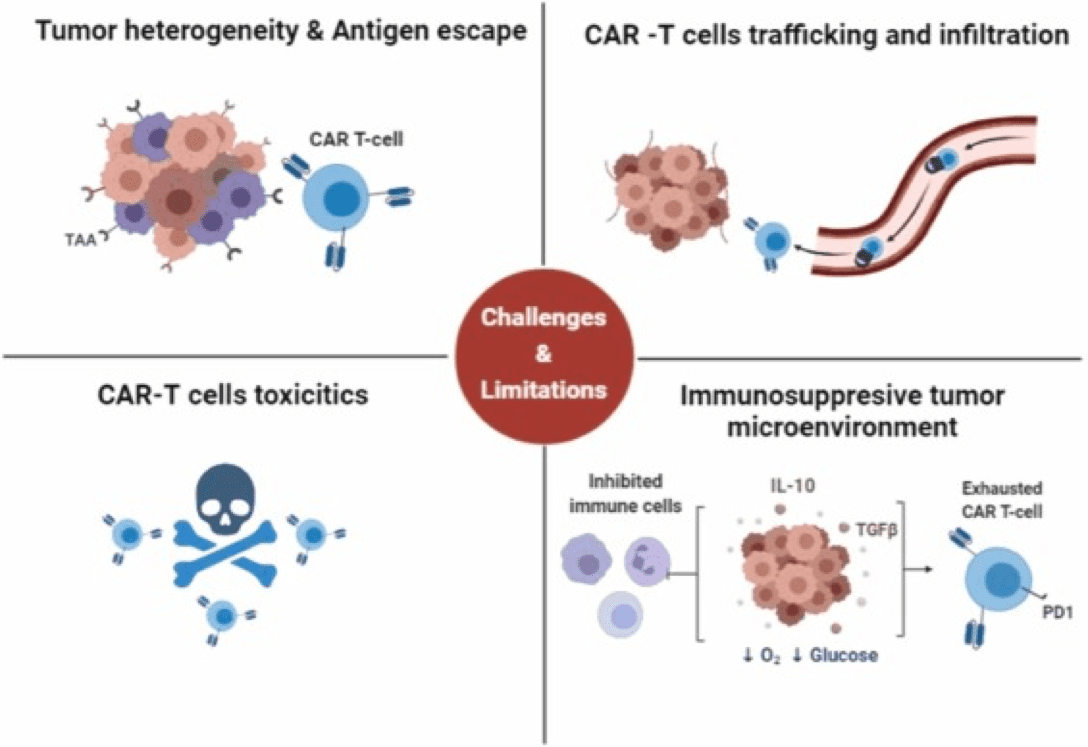
ในขณะที่การบำบัดด้วยเซลล์ CAR T-cell ประสบความสำเร็จอย่างมากในการรักษามะเร็งเม็ดเลือด นักวิจัยก็กำลังสำรวจความเป็นไปได้ในการใช้งานกับมะเร็งชนิดอื่นๆ รวมถึงเนื้องอกที่เป็นก้อน อย่างไรก็ตาม การพัฒนาของการบำบัดด้วยเซลล์ CAR T-cell สำหรับเนื้องอกที่เป็นของแข็งนั้นมีความท้าทายหลายประการ ความท้าทายประการหนึ่งคือสภาพแวดล้อมจุลภาคที่ซับซ้อนและแอนติเจนจำเพาะที่น้อยลงบนพื้นผิวของเนื้องอกที่เป็นของแข็งเหล่านี้ การขาดแอนติเจนเฉพาะบนก้อนเนื้องอกทำให้ยากที่จะกำหนดเป้าหมายเซลล์เนื้องอกโดยไม่ทำอันตรายต่อเนื้อเยื่อปกติ นอกจากนี้ เนื่องจากเนื้องอกที่เป็นของแข็งมีความแตกต่างกันอย่างมาก จึงทำให้ยากต่อการระบุและกำหนดเป้าหมายเซลล์เนื้องอกด้วย CAR T-cells สภาพแวดล้อมขนาดเล็กของเนื้องอกภูมิคุ้มกันในเนื้องอกที่เป็นของแข็งยังสามารถยับยั้งการทำงานของทีเซลล์และทำให้มีประสิทธิภาพน้อยลง CAR T-cells ที่ออกแบบมาเพื่อกำหนดเป้าหมายแอนติเจนที่แสดงออกบนเซลล์เนื้องอกที่เป็นของแข็งอาจจดจำและโจมตีเซลล์ที่มีสุขภาพที่แสดงแอนติเจนที่คล้ายกันหรือเหมือนกัน ส่งผลให้เกิดความเป็นพิษนอกเป้าหมาย นอกจากนี้ยังอาจเป็นเรื่องท้าทายสำหรับ CAR T-cell ในการจราจรและแทรกซึมเข้าไปในเนื้องอก ซึ่งจำกัดความสามารถในการกำหนดเป้าหมายและฆ่าเซลล์เนื้องอก
ความท้าทายในการบำบัดด้วยเซลล์ CAR T-cell ในเนื้องอกที่เป็นของแข็ง เครดิต: Mehrabadi AZ, Ranjbar R, Farzanehpour M และอื่น ๆ doi:10.1016/j.biopha.2021.112512 ทำซ้ำภายใต้ สัญญาอนุญาตครีเอทีฟคอมมอนส์
ภาพรวมโดยย่อของ การบำบัดด้วย TCR-T
ซึ่งแตกต่างจาก CAR T-cells T เซลล์ที่ออกแบบโดย TCR จดจำเปปไทด์ที่นำเสนอโดย MHC ที่ได้มาจากโปรตีนของช่องเซลล์ทั้งหมด เนื้องอกที่เป็นก้อนจำนวนมากไม่ได้แสดงแอนติเจนที่พื้นผิว แต่จะแสดงแอนติเจนของเนื้องอกในเซลล์ ด้วยเหตุนี้ การบำบัดด้วย TCR-T จึงอาจเหมาะสมกว่าการบำบัดด้วย CAR T-cell ในการรักษาเนื้องอกที่เป็นก้อน ซึ่งประกอบขึ้นเป็นมะเร็งส่วนใหญ่
พื้นที่ การทดลองทางคลินิก สำหรับการรักษา TCR ของเนื้องอกที่เป็นของแข็งได้ดำเนินการเป็นครั้งแรกสำหรับผู้ป่วยที่เป็นมะเร็งผิวหนัง ตั้งแต่นั้นมา มีการทดลองทางคลินิกมากมายสำหรับการรักษามะเร็งชนิดต่างๆ รวมถึงมะเร็งซาร์โคมา มะเร็งเซลล์ไต กระเพาะปัสสาวะ ปอด หลอดอาหาร มะเร็งระยะแพร่กระจาย มะเร็งตับอ่อน และมะเร็งตับ
หนึ่งในความท้าทายของการบำบัดด้วย TCR-T คือการระบุแอนติเจนที่เหมาะสมเพื่อกำหนดเป้าหมาย สิ่งนี้ต้องการความเข้าใจอย่างลึกซึ้งเกี่ยวกับมะเร็งเฉพาะที่เป็นเป้าหมาย เช่นเดียวกับรูปแบบการแสดงออกของแอนติเจนบนเซลล์มะเร็ง นอกจากนี้ยังมีความเสี่ยงที่จะเกิดผลนอกเป้าหมาย โดยที่ T เซลล์ที่ถูกดัดแปลงจะโจมตีเซลล์ที่มีสุขภาพนอกเหนือจากเซลล์มะเร็ง แม้จะมีความท้าทายเหล่านี้ การบำบัดด้วย TCR-T ได้แสดงให้เห็นผลลัพธ์ที่คาดหวังในการทดลองทางคลินิกระยะแรก การบำบัดด้วย TCR-T ยังคงเป็นแนวทางที่ค่อนข้างใหม่ในการรักษามะเร็ง และจำเป็นต้องมีการวิจัยเพิ่มเติมเพื่อให้เข้าใจถึงประโยชน์และข้อจำกัดที่เป็นไปได้อย่างถ่องแท้
ความแตกต่างระหว่างการบำบัดด้วยเซลล์ CAR T-cell และการบำบัดด้วย TCR-T
คาร์ ที-เซลล์ บำบัด การบำบัดด้วย TCR-T สร้าง - ตัวรับที่ได้รับการออกแบบทางวิศวกรรมประกอบด้วยโดเมนภายในเซลล์และนอกเซลล์ – TCR แบบเนทีฟหรือได้รับการออกแบบทางวิศวกรรมน้อยที่สุด เป้าหมาย – กำหนดเป้าหมายแอนติเจนที่ผิวเซลล์เท่านั้น – กำหนดเป้าหมายทั้งผิวเซลล์และแอนติเจนภายในเซลล์ที่แสดงโดยโมเลกุลระดับ MHC ข้อดี – เป้าหมายเซลลูล่าร์ไม่ถูกจำกัดโดยคอมเพล็กซ์ MHC – เปิดใช้งานเป้าหมายที่หลากหลายมากขึ้นเนื่องจากสามารถกำหนดเป้าหมายแอนติเจนภายในเซลล์ได้ ข้อเสีย – มีผลเพียงเล็กน้อยต่อเนื้องอกที่เป็นของแข็ง – ถูกจำกัดโดยความเข้ากันได้ของ MHC สถานะองค์การอาหารและยา - การรักษาที่ได้รับการอนุมัติสำหรับมะเร็งหลายรูปแบบ – อยู่ระหว่างการทดลองทางคลินิก
โดยรวมแล้ว ทั้งการบำบัดด้วยเซลล์ CAR T-cell และการบำบัดด้วย TCR-T แสดงถึงการพัฒนาที่น่าตื่นเต้นในด้านภูมิคุ้มกันบำบัดมะเร็ง ซึ่งนำเสนอศักยภาพในการรักษามะเร็งหลากหลายชนิดและปรับปรุงผลลัพธ์สำหรับผู้ป่วย แม้ว่าทั้งสองวิธีจะมีความแตกต่างที่สำคัญบางประการ แต่ทั้งสองวิธีก็มีจุดแข็งและความท้าทายที่แตกต่างกันไป และทั้งสองวิธีมีศักยภาพในการสร้างผลกระทบอย่างมีนัยสำคัญต่อการรักษาโรคมะเร็ง แม้ว่าจะมีความท้าทายที่ต้องแก้ไข แต่นักวิจัยยังคงสำรวจศักยภาพของการบำบัดที่เป็นนวัตกรรมเหล่านี้ต่อไป เราคาดหวังที่จะเห็นความก้าวหน้าที่สำคัญในการต่อสู้กับโรคมะเร็งในอีกหลายปีข้างหน้า
อ้างอิง: อิวิกา, นาซี; Young, CM ติดตามการปฏิวัติ CAR-T: การวิเคราะห์การทดลองทางคลินิกของการบำบัดด้วย CAR-T และ TCR-T สำหรับการรักษาโรคมะเร็ง (1997-2020) การดูแลสุขภาพ 2021, 9 , 1062. https://doi.org/10.3390/healthcare9081062
Mehrabadi AZ, Ranjbar R, Farzanehpour M และคณะ ศักยภาพการรักษาของเซลล์ CAR T ในมะเร็ง: การทบทวนขอบเขต เภสัชกรไบโอเมด . 2022;146:112512. doi:10.1016/j.biopha.2021.112512
Shafer P, Kelly LM, Hoyos V. การบำบัดมะเร็งด้วยทีเซลล์ที่ออกแบบโดย TCR: กลยุทธ์ปัจจุบัน ความท้าทาย และอนาคต หน้าอิมมูโนล . 2022;13:835762. เผยแพร่ 2022 มี.ค. 3 doi:10.3389/fimmu.2022.835762
Zhang, Y., Liu, Z., Wei, W. และคณะ TCR ออกแบบทีเซลล์สำหรับการรักษาด้วยภูมิคุ้มกันเนื้องอกที่เป็นของแข็ง Exp Hematol Oncol 11, 38 (2022) https://doi.org/10.1186/s40164-022-00291-0