เซลล์ต้นกำเนิดมีเซนไคมอล (MSCs) กระตุ้นความสนใจอย่างมากเนื่องจากมีคุณสมบัติในการกระตุ้นภูมิคุ้มกันและต้านการอักเสบ และมีแนวโน้มที่ดีในด้านเวชศาสตร์ฟื้นฟูและการบำบัดด้วยภูมิคุ้มกัน
เพื่อเพิ่มประสิทธิภาพของ MSCs ในฐานะการบำบัดด้วยเซลล์ การกำหนดกลไกที่พวกมันออกฤทธิ์กระตุ้นภูมิคุ้มกันจึงเป็นสิ่งสำคัญ แม้ว่าเส้นทางที่แม่นยำในการควบคุมการกระทำของการปรับภูมิคุ้มกันของ MSC ยังคงยากลำบาก แต่หลักฐานที่สะสมก็ชี้ไปที่ความสามารถในการระงับการตอบสนองของระบบภูมิคุ้มกัน ผ่านทาง ปฏิสัมพันธ์ระหว่างเซลล์โดยตรงและการหลั่งโมเลกุลควบคุมภูมิคุ้มกัน
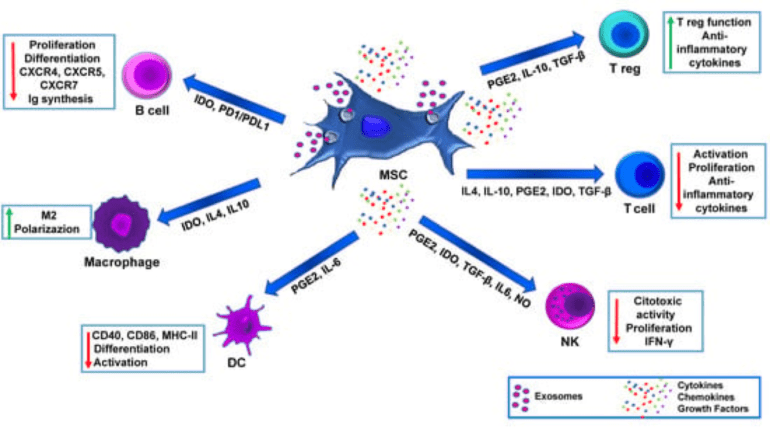
2 รูป: ผลการกระตุ้นภูมิคุ้มกันของ MSCdoi.org/10.3390/biomedicines11051426 สัญญาอนุญาตครีเอทีฟคอมมอนส์ ต่อไปนี้เป็นกลไกสำคัญบางส่วนที่ MSC ออกฤทธิ์กระตุ้นภูมิคุ้มกัน:
การปราบปรามการเพิ่มจำนวนทีเซลล์:
MSC สามารถยับยั้งการแพร่กระจายและการกระตุ้นของทีเซลล์ ซึ่งเป็นส่วนสำคัญในการตอบสนองของระบบภูมิคุ้มกันแบบปรับตัวได้ พวกมันสามารถปรับการตอบสนองของทีเซลล์ทั้ง CD4+ และ CD8+ ได้ ดังนั้นจึงทำให้ปฏิกิริยาภูมิคุ้มกันลดลง
การควบคุมของเซลล์ B:
MSC สามารถมีอิทธิพลต่อการทำงานของบีเซลล์ รวมถึงการเพิ่มจำนวน การเปลี่ยนสภาพ และการหลั่งของแอนติบอดี สามารถยับยั้งการสร้างพลาสมาเซลล์และการผลิตแอนติบอดีได้
การเหนี่ยวนำของทีเซลล์ควบคุม (Tregs):
MSC ส่งเสริมการสร้างและการขยายตัวของทีเซลล์ควบคุม (Tregs) ซึ่งมีความสำคัญอย่างยิ่งต่อการรักษาความทนทานของระบบภูมิคุ้มกันและระงับการตอบสนองของระบบภูมิคุ้มกันที่มากเกินไป
การปรับเซลล์ Dendritic (DCs):
MSC สามารถเปลี่ยนการเจริญเติบโตและการทำงานของเซลล์เดนไดรต์ ซึ่งเป็นเซลล์ที่สร้างแอนติเจนซึ่งมีความสำคัญอย่างยิ่งต่อการเริ่มต้นการตอบสนองทางภูมิคุ้มกันแบบปรับตัว MSC สามารถชักนำฟีโนไทป์ที่ยอมรับได้ใน DC ซึ่งลดความสามารถในการกระตุ้นการกระตุ้นทีเซลล์
การหลั่งโมเลกุลต้านการอักเสบ:
MSC ผลิตและปล่อยโมเลกุลต้านการอักเสบต่างๆ เช่น พรอสตาแกลนดิน E2 (PGE2), เปลี่ยนปัจจัยการเจริญเติบโต-เบต้า (TGF-β), อินโดลามีน 2,3-ไดออกซีเจเนส (IDO), อินเตอร์ลิวคิน-10 (IL-10) และเซลล์ตับ ปัจจัยการเจริญเติบโต (HGF) โมเลกุลเหล่านี้สามารถระงับการอักเสบและปรับการทำงานของเซลล์ภูมิคุ้มกันได้
ปฏิสัมพันธ์กับเซลล์ภูมิคุ้มกันโดยกำเนิด:
MSC สามารถโต้ตอบกับเซลล์ภูมิคุ้มกันโดยกำเนิด ซึ่งรวมถึงเซลล์มาโครฟาจและเซลล์นักฆ่าตามธรรมชาติ (NK) ซึ่งมีอิทธิพลต่อการกระตุ้นและการทำงานของพวกมัน MSC สามารถส่งเสริมโพลาไรเซชันของมาโครฟาจไปสู่ฟีโนไทป์ M2 ที่ต้านการอักเสบ
โมเดลเมาส์ที่มนุษย์สร้างขึ้น การใช้แบบจำลองเมาส์ในการศึกษาพรีคลินิกแสดงถึงขั้นตอนสำคัญในการประเมินและการเพิ่มประสิทธิภาพของผลกระทบทางภูมิคุ้มกันของ MSC ก่อนการแปลทางคลินิก แบบจำลองเมาส์นำเสนอแพลตฟอร์มที่มีคุณค่าสำหรับการตรวจสอบความปลอดภัย ประสิทธิภาพ และกลไกที่เป็นรากฐานของการแทรกแซงที่ใช้ MSC ในห้องปฏิบัติการที่ได้รับการควบคุม แบบจำลองเหล่านี้ช่วยให้นักวิจัยสามารถจำลองสภาวะของโรคต่างๆ และการตอบสนองของภูมิคุ้มกัน โดยให้ข้อมูลเชิงลึกเกี่ยวกับการประยุกต์ใช้ MSC ในการรักษาที่เป็นไปได้ในความผิดปกติต่างๆ รวมถึงโรคภูมิต้านตนเอง ภาวะการอักเสบ และการบาดเจ็บของเนื้อเยื่อ
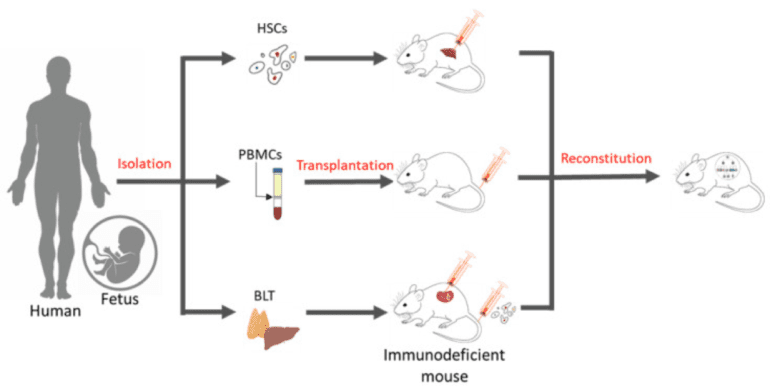
2 รูป: วิธีการต่างๆ ในการสร้างหนูที่มีลักษณะเหมือนมนุษย์ 10.3390/เภสัช15061600 สัญญาอนุญาตครีเอทีฟคอมมอนส์
หนูที่มีมนุษยธรรม มีการใช้มากขึ้นเป็นแบบจำลองในการศึกษาโรคที่เกิดจากระบบภูมิคุ้มกัน เนื่องจากจำลองภูมิคุ้มกันวิทยาของมนุษย์ได้ใกล้กว่าแบบจำลองของหนูทั่วไป พวกหนูเหล่านี้คือ หนูที่มีภาวะภูมิคุ้มกันบกพร่อง ซึ่งระบบภูมิคุ้มกันถูกสร้างขึ้นใหม่ด้วยเซลล์ภูมิคุ้มกันของมนุษย์ หนูที่มีลักษณะเหมือนมนุษย์เหล่านี้ทำหน้าที่เป็นเครื่องมือในการพัฒนาความเข้าใจที่ดีขึ้นเกี่ยวกับรูปแบบการออกฤทธิ์ของ MSC ในการบรรเทาการตอบสนองของระบบภูมิคุ้มกันใน ในร่างกาย สภาพแวดล้อมที่มีลักษณะใกล้เคียงกับวิทยาภูมิคุ้มกันของมนุษย์ ต่อไปนี้เป็นประเภทเมาส์ที่มีลักษณะเหมือนมนุษย์ทั่วไปบางประเภท:
เซลล์โมโนไซต์ในเลือดของมนุษย์ (PBMC) หนูที่ปลูกถ่าย :
หนูเหล่านี้ถูกสร้างขึ้นโดยการฉีดเซลล์โมโนไซต์ในเลือดของมนุษย์ (PBMC ) ไปในหนูที่มีภาวะภูมิคุ้มกันบกพร่อง PBMC ปลูกถ่ายและเติมเลือดบริเวณรอบข้างของเมาส์ ซึ่งเป็นแบบจำลองระยะสั้นเพื่อศึกษาการตอบสนองของระบบภูมิคุ้มกันของมนุษย์
เซลล์ต้นกำเนิดเม็ดเลือดของมนุษย์ CD34+ (CD34+ HSC) หนูเมาส์:
CD34+ HSC หนูถูกสร้างขึ้นโดยการปลูกถ่ายหนูที่มีภาวะภูมิคุ้มกันบกพร่องด้วย CD34+ HSC ของมนุษย์ซึ่งโดยทั่วไปได้มาจากเลือดจากสายสะดือ ซึ่งส่งผลให้เกิดการพัฒนาระบบภูมิคุ้มกันของมนุษย์ภายในหนู รวมถึงทีเซลล์ บีเซลล์ และเซลล์ไมอีลอยด์
ไขกระดูก, ตับ, ไธมัส (BLT) หนูเมาส์ที่มีลักษณะเหมือนมนุษย์:
หนูที่มีลักษณะคล้ายมนุษย์ของ BLT ถูกสร้างขึ้นโดยการปลูกถ่ายตับของทารกในครรภ์และเนื้อเยื่อไทมัสของมนุษย์ไว้ใต้แคปซูลไต และฉีดเซลล์ต้นกำเนิดเม็ดเลือด CD34+ ของมนุษย์เข้าไปในหนู แบบจำลองนี้สนับสนุนการพัฒนาระบบภูมิคุ้มกันของมนุษย์ที่สมบูรณ์ยิ่งขึ้น รวมถึงการศึกษาทีเซลล์ในสภาพแวดล้อมไทมัสของมนุษย์
1 ตาราง: การเปรียบเทียบระหว่าง CD34+, PBMC และ BLT ทำให้เกิดหนูเมาส์ที่ถูกทำให้มีลักษณะของมนุษย์
ซีดี34+ พีบีเอ็มซี BLT การฉีดเซลล์ CD34+ จากเลือดจากสายสะดือ/ตับทารกในครรภ์ การฉีด PBMC ของมนุษย์ในช่องท้อง การปลูกถ่ายร่วมกันของทารกในครรภ์ thy/liv ด้วยการฉีด iv ของเซลล์ CD34+ จากเลือดจากสายสะดือ/ตับของทารกในครรภ์ – ง่ายต่อการจัดตั้ง – ง่ายต่อการจัดตั้ง – การสร้างเม็ดเลือดหลายสาย
หนูที่มีลักษณะเหมือนมนุษย์เป็นแบบจำลองในการศึกษาผลกระทบทางภูมิคุ้มกันของ MSC หนูที่มีลักษณะเหมือนมนุษย์ทำหน้าที่เป็นแบบจำลองอันล้ำค่าในการตรวจสอบผลกระทบทางภูมิคุ้มกันของ MSC ก่อนที่จะนำไปใช้ทางคลินิก เนื่องจาก MSC ที่ใช้ในสถานพยาบาลมักมีต้นกำเนิดมาจากแหล่งอัลโลจีนิก จึงมีศักยภาพที่จะกระตุ้นการตอบสนองทางภูมิคุ้มกันในผู้รับ ดังนั้นจึงจำเป็นอย่างยิ่งที่จะต้องประเมินภูมิคุ้มกันและโปรไฟล์ความปลอดภัยของ MSC ในแบบจำลองเมาส์พรีคลินิก โดยหนูที่มีลักษณะเหมือนมนุษย์ได้รับการพิสูจน์ว่าเป็นประโยชน์อย่างยิ่งต่อจุดประสงค์นี้
ใน การศึกษาการประเมินความปลอดภัย โดย Lee เอตอัล แบบจำลองเมาส์ที่มีลักษณะของมนุษย์ถูกสร้างขึ้นโดยการฉีดเซลล์ CD34+ ในหลอดเลือดดำเข้าไปในหนู NOD/SCID IL2γnull (NSG) ที่มีภาวะภูมิคุ้มกันบกพร่องเพื่อตรวจสอบความปลอดภัยทางภูมิคุ้มกันวิทยาของ MSC ของมนุษย์ที่เป็นอัลโลจีนิก ผลการวิจัยชี้ให้เห็นว่า MSC ที่ได้มาจากสายสะดือแบบ allogeneic มีภูมิคุ้มกันต่ำทั้งสองอย่าง ในหลอดทดลอง และ ในร่างกาย ดังนั้นจึงถือว่า “ปลอดภัยทางภูมิคุ้มกัน” สำหรับการใช้งานทางคลินิกแบบอัลโลจีนิก
อื่น ศึกษา โดย Roeming-van Rhijn และคณะ สำรวจการใช้ MSC เป็นวิธีการรักษาทางเลือกอื่นสำหรับการปฏิเสธการปลูกถ่าย allograft พวกเขาประเมินประสิทธิภาพการปรับภูมิคุ้มกันของ MSC ที่ได้มาจากไขกระดูก (BM-MSCs) และ MSC ที่ได้มาจากเนื้อเยื่อไขมัน (AT-MSCs) ในแบบจำลองเมาส์ที่มีภูมิคุ้มกันบกพร่องแบบผสมผสานเซิร์ฟเวอร์ PBMC (SCID) ที่ถูกปลูกถ่ายด้วยการปลูกถ่ายผิวหนังมนุษย์ที่มีลักษณะเป็นอัลโลจีนิก ผลลัพธ์แสดงให้เห็นว่าทั้ง BM-MSC และ AT-MSC ระงับฤทธิ์อัลโลแอคติวิตีต่อการปลูกถ่ายผิวหนังได้อย่างมีประสิทธิภาพ โดยเน้นถึงศักยภาพของแบบจำลอง SCID-PBMC ที่สร้างโดยมนุษย์ในการประเมินประสิทธิภาพการกดภูมิคุ้มกันของ MSC ในสถานการณ์การปฏิเสธการปลูกถ่าย allograft
ในบริบทของการรักษาโรคที่เกิดจากการรับสินบนเทียบกับเจ้าบ้าน (GvHD) ซึ่งเป็นภาวะแทรกซ้อนที่รุนแรงหลังการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดชนิดอัลโลจีนิก (HSCT) หนูเมาส์ที่มีลักษณะของมนุษย์ของ NSG-PBMC ทำหน้าที่เป็นแบบจำลองที่เกี่ยวข้องสำหรับ aGvHD ใน ศึกษา ที่ได้กล่าวถึง การบำบัดด้วยเซลล์ MSC ของมนุษย์ช่วยยืดอายุการอยู่รอดของหนู NSG ที่มี aGvHD ได้อย่างมีนัยสำคัญ ขณะเดียวกันก็ลดพยาธิสภาพของอวัยวะเป้าหมาย สิ่งนี้เน้นย้ำถึงประโยชน์ของหนู NSG-PBMC GvHD ซึ่งเป็นแบบจำลองที่เหมาะสมสำหรับการอธิบายกลไกที่เป็นพื้นฐานของการกดภูมิคุ้มกันของ MSC และการประเมินศักยภาพของ MSC ในการรักษาโดยใช้เซลล์สำหรับ GvHD
การใช้แบบจำลองเมาส์ที่มีลักษณะเหมือนมนุษย์แสดงถึงความก้าวหน้าที่สำคัญในการประเมินผลกระทบทางภูมิคุ้มกันของ MSC ก่อนที่จะแปลผลทางคลินิก การศึกษาที่กล่าวถึงเน้นย้ำถึงความสำคัญของการประเมินภูมิคุ้มกันและประวัติความปลอดภัยของ MSCs โดยเฉพาะอย่างยิ่งในบริบทของการปลูกถ่ายอัลโลจีนิก ซึ่งมีความเสี่ยงที่จะถูกปฏิเสธโดยภูมิคุ้มกันเพิ่มมากขึ้น การประเมินดังกล่าวช่วยอำนวยความสะดวกในการตรวจสอบคุณสมบัติการปรับภูมิคุ้มกันของ MSC และประโยชน์ในการรักษาที่เป็นไปได้ของคุณสมบัติเหล่านี้ในการจัดการกับสภาวะต่างๆ เช่น การปฏิเสธการปลูกถ่ายอวัยวะและ GvHD ข้อค้นพบจากการศึกษาเหล่านี้ให้ข้อมูลเชิงลึกที่มีคุณค่าเกี่ยวกับประสิทธิภาพ ความปลอดภัย และกลไกที่เป็นรากฐานของการรักษาโดยใช้ MSC ซึ่งเป็นแนวทางในการพัฒนาวิธีการรักษาระดับเซลล์รูปแบบใหม่ พร้อมเพิ่มประสิทธิภาพทางคลินิกและลดผลข้างเคียง ในอนาคตข้างหน้า การวิจัยอย่างต่อเนื่องในโมเดลเมาส์ที่มนุษย์สร้างขึ้นจะมีบทบาทสำคัญในการพัฒนาความเข้าใจของเราเกี่ยวกับอิมมูโนชีววิทยาของ MSC และอำนวยความสะดวกในการแปลการรักษาโดยใช้ MSC จากแบบตั้งโต๊ะไปจนถึงข้างเตียง ซึ่งท้ายที่สุดจะนำเสนอแนวทางใหม่ในการรักษาโรคที่ทำให้ร่างกายอ่อนแอและปรับปรุงผลลัพธ์ของผู้ป่วย
อ้างอิง:
บาราชินี ส.; บีโซ, ล.; โกลาชาลัม ส.; เพทรินี ไอ.; แม็กจิโอ ร.; สการ์เซลลี ม.; Longoni, B. Mesenchymal Stem Cell ในการปลูกถ่ายเกาะเล็กตับอ่อน ชีวการแพทย์ 2023, 11 , 1426. https://doi.org/10.3390/biomedicines11051426
Karnik I, Her Z, Neo SH, Liu WN, Chen Q. การใช้งานพรีคลินิกที่เกิดขึ้นใหม่ของโมเดลเมาส์ Humanized ในการค้นพบและการตรวจสอบความถูกต้องของการบำบัดด้วยภูมิคุ้มกันแบบใหม่และกลไกการออกฤทธิ์เพื่อปรับปรุงการรักษามะเร็ง เภสัชกรรม. 2023 26 พ.ค.;15(6):1600 น. ดอย: 10.3390/เภสัช15061600.
Lee M, Jeong SY, Ha J และคณะ ภูมิคุ้มกันต่ำของเซลล์ต้นกำเนิดมีเซนไคมัลที่ได้มาจากเลือดจากสายสะดือของมนุษย์ ในหลอดทดลอง และ ในร่างกาย ชุมชน Biochem Biophys Res 2014;446(4):983-989. ดอย:10.1016/j.bbrc.2014.03.051
Mehler VJ, เบิร์นส์ ซี, มัวร์ ML. บทวิจารณ์โดยย่อ: การสำรวจคุณลักษณะภูมิคุ้มกันของเซลล์มีเซนไคมัลสโตรมัลในแบบจำลองเมาส์ที่มีลักษณะของมนุษย์ เซลล์ต้นกำเนิด. 2019;37(3):298-305. ดอย:10.1002/stem.2948
โรเมลิง-แวน ไรจ์น เอ็ม, ไครูน เอ็ม, โคเรวาร์ เอสเอส และคณะ เซลล์สโตรมัลมีเซนไคมอลที่ได้มาจากไขกระดูกของมนุษย์และเนื้อเยื่อไขมันเป็นเซลล์ภูมิคุ้มกัน ในหลอดทดลอง และในรูปแบบการปฏิเสธการปลูกถ่ายอัลโลกราฟต์โดยมนุษย์ เจ สเต็มเซลล์ เรส เธอ 2013;เอกสาร 6(1):20780. ดอย:10.4172/2157-7633.S6-001
Tobin LM, Healy ME, English K, Mahon BP เซลล์ต้นกำเนิดมีเซนไคม์ของมนุษย์ยับยั้งการแพร่กระจายของทีเซลล์ CD4(+) ของผู้บริจาคและลดพยาธิวิทยาในแบบจำลองหนูเมาส์ที่ทำให้มีลักษณะของมนุษย์ของโรคเจ้าบ้านที่รับสินบนเฉียบพลันเทียบกับเจ้าบ้าน คลินิก เอ็กซ์พี อิมมูนอล 2013;172(2):333-348. ดอย:10.1111/cei.12056
วู เอช, เหวิน ดี, มาฮาโตะ โรดไอ. เซลล์ต้นกำเนิดจากเนื้อเยื่ออ่อนของบุคคลที่สามปรับปรุงการปลูกถ่ายเกาะเล็กเกาะน้อยของมนุษย์ในแบบจำลองเมาส์เบาหวานที่มนุษย์สร้างขึ้น โมล เธอ. 2013;21(9):1778-1786. ดอย:10.1038/mt.2013.147
Zhao Q, Ren H, Han Z. เซลล์ต้นกำเนิด Mesenchymal: ความสามารถในการกระตุ้นภูมิคุ้มกันและศักยภาพทางคลินิกในโรคภูมิคุ้มกัน เจ เซลล์ ภูมิคุ้มกัน 2016;2:3–20. ดอย:10.1016/j.jocit.2014.12.001
โจวซี ไป๋ XY กลยุทธ์ในการชักนำให้เกิดเซลล์ต้นกำเนิดจากเยื่อหุ้มเซลล์ต้านการอักเสบ และการประยุกต์ใช้ในการรักษาโรคไตที่เกิดจากระบบภูมิคุ้มกัน ฟรอนต์เมด (โลซาน) 2022 ส.ค. 19;9:891065. ดอย:10.3389/fmed.2022.891065.