[Vc_row] [vc_column] [vc_column_text]
iPSC คืออะไร?
ชักนำเซลล์ต้นกำเนิด pluripotent (iPSCs) เป็นสเต็มเซลล์ชนิดหนึ่งที่ได้มาจากเซลล์ร่างกายผู้ใหญ่ เช่น ผิวหนังหรือเซลล์เม็ดเลือด พวกมันถูกสร้างขึ้นโดยการตั้งโปรแกรมใหม่ให้กับเซลล์ของผู้ใหญ่ให้อยู่ในสถานะที่มีพลังคล้ายเอ็มบริโอซึ่งช่วยให้สามารถพัฒนาแหล่งที่มาของเซลล์ชนิดใดก็ได้ในร่างกายมนุษย์อย่างไม่จำกัด iPSCs ถูกค้นพบครั้งแรกในปี 2006 โดยทีมนักวิจัยที่นำโดย Shinya Yamanaka จากมหาวิทยาลัยเกียวโต ประเทศญี่ปุ่น ซึ่งได้รับรางวัล รางวัลโนเบล สำหรับงานของเขาเกี่ยวกับ iPSC ในปี 2012
iPSC ถูกสร้างขึ้นอย่างไร?
iPSCs ถูกสร้างขึ้นผ่านกระบวนการที่เรียกว่า reprogramming ซึ่งเกี่ยวข้องกับการแนะนำยีนเฉพาะเข้าสู่เซลล์ร่างกายของผู้ใหญ่โดยใช้เทคนิคทางพันธุวิศวกรรมรวมถึงการถ่ายทอดไวรัส สี่ยีนที่ใช้โดยทั่วไปสำหรับการเขียนโปรแกรมซ้ำ ได้แก่ Oct4, Sox2, Klf4 และ c-Myc จากนั้นเซลล์ที่ทรานส์เฟกจะถูกบ่มบนชั้นฟีดเดอร์ภายใต้สภาวะที่เหมาะสมของอาหารเลี้ยงเชื้อ และหลังจากการแสดงออกของปัจจัยการตั้งโปรแกรมซ้ำ เซลล์จะรีเซ็ตเป็นสถานะคล้ายตัวอ่อน จากนั้น iPSCs ที่เป็นผลลัพธ์สามารถนำไปเพาะเลี้ยงและนำไปแยกประเภทเซลล์เฉพาะ เช่น เซลล์หัวใจหรือเซลล์ประสาท
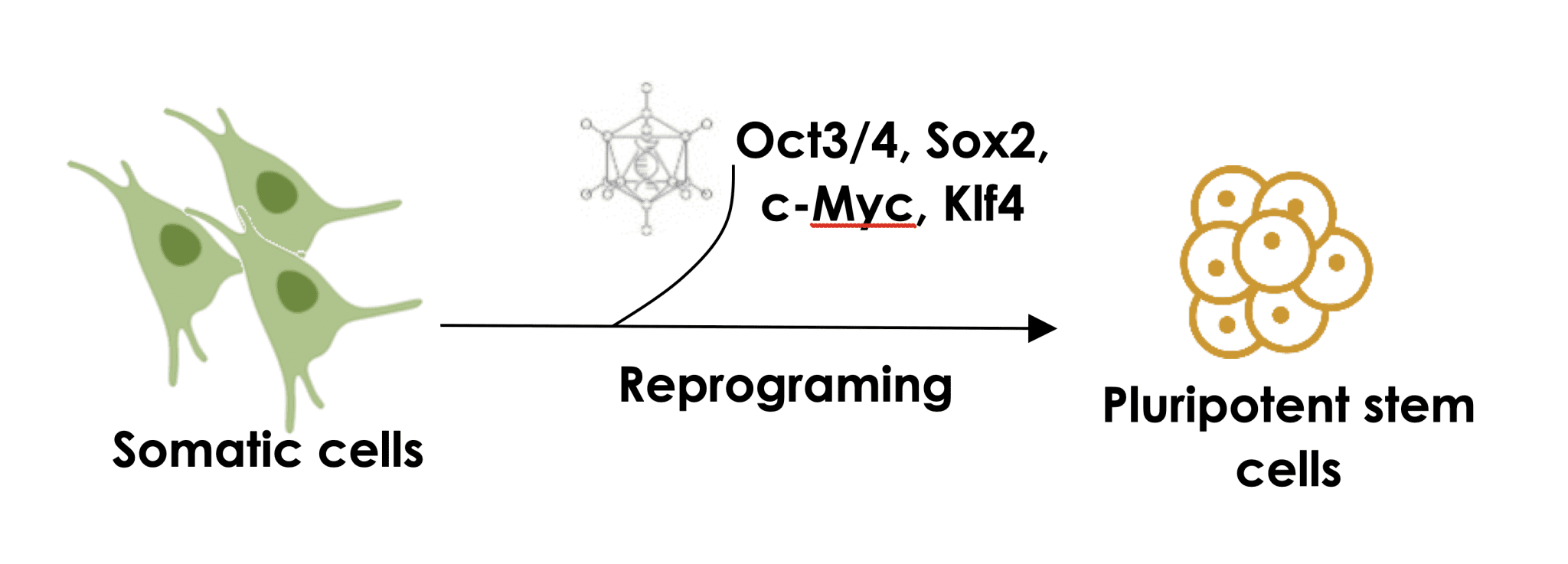 การสร้างโปรแกรมเซลล์ร่างกายใหม่ให้เป็นเซลล์ต้นกำเนิดหลายเซลล์โดยการนำปัจจัยการปรับโปรแกรมใหม่
การสร้างโปรแกรมเซลล์ร่างกายใหม่ให้เป็นเซลล์ต้นกำเนิดหลายเซลล์โดยการนำปัจจัยการปรับโปรแกรมใหม่
แอพพลิเคชั่นของ iPSC คืออะไร?
iPSCs มีการใช้งานที่หลากหลายในด้านการวิจัยและการแพทย์ หนึ่งในสาขาการวิจัยที่มีแนวโน้มมากที่สุดคือการสร้างแบบจำลองโรค เนื่องจาก iPSC สามารถต่ออายุได้เอง เซลล์เหล่านี้จึงสามารถแยกความแตกต่างออกเป็นเซลล์ทุกประเภทได้อย่างง่ายดาย ซึ่งสามารถนำไปใช้ในการจัดทำแบบจำลองโรคเพื่อศึกษาโรคเหล่านั้นได้ ตัวอย่างเช่น สามารถสร้าง iPSC จากผู้ป่วยที่มีโรคทางพันธุกรรมหรือโรคที่ซับซ้อน เช่น อัลไซเมอร์และพาร์กินสัน ซึ่งช่วยให้นักวิจัยเข้าใจกลไกของโรคได้ดีขึ้นและพัฒนาวิธีการรักษาใหม่ๆ
iPSCs ยังถูกใช้ในการค้นพบยาหรือการศึกษาความเป็นพิษต่อเซลล์ สามารถใช้เพื่อคัดกรองสารประกอบจำนวนมากสำหรับความสามารถในการรักษาโรคเฉพาะ ซึ่งสามารถเร่งกระบวนการพัฒนายาและลดความจำเป็นในการทดสอบกับสัตว์ iPSC ยังใช้ในการทดสอบทางพิษวิทยาเพื่อระบุสารประกอบที่เป็นพิษ ซึ่งเสนอทางเลือกอื่นแทนการทดสอบในสัตว์เพื่อการประเมินความปลอดภัยของสารเคมีที่ดีขึ้น
ในเซลล์บำบัดและเวชศาสตร์ฟื้นฟู iPSCs มีศักยภาพในการรักษาโรคและอาการต่างๆ มากมาย สามารถใช้เพื่อสร้างเซลล์ที่แข็งแรงเพื่อทดแทนเนื้อเยื่อที่เสียหายหรือเป็นโรค ซึ่งสามารถใช้รักษาภาวะต่างๆ เช่น โรคหัวใจ เบาหวาน และไขสันหลังได้
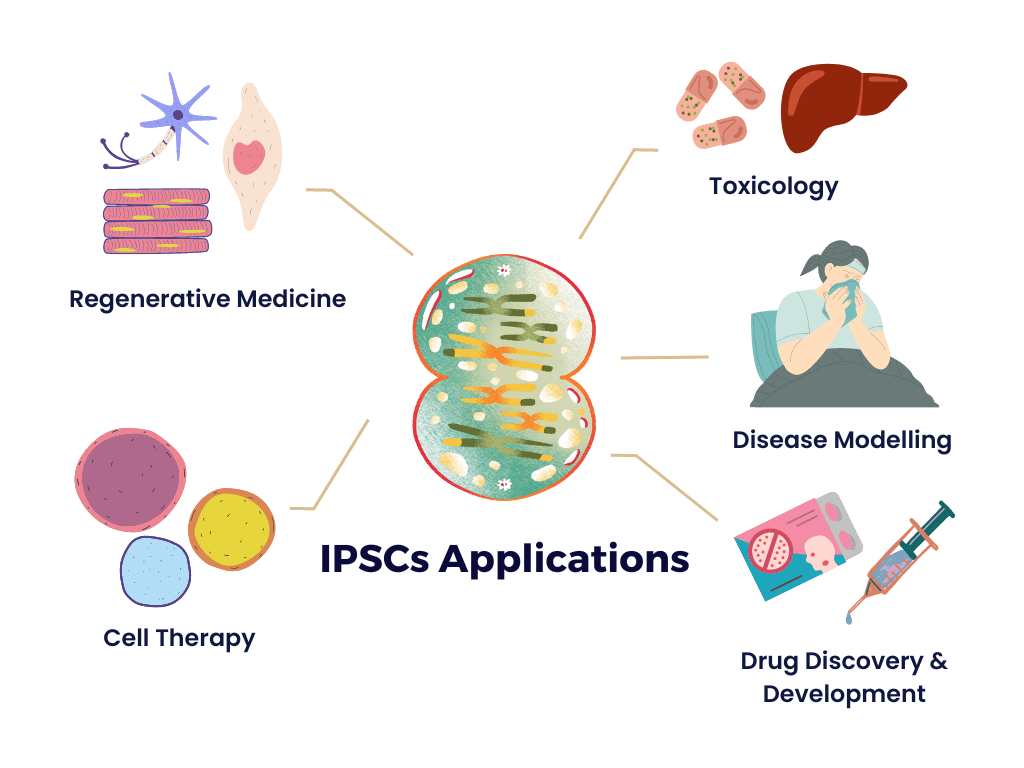 การประยุกต์ใช้เซลล์ต้นกำเนิดพลูริโพเทนท์ (IPSCs) ในทางการแพทย์
การประยุกต์ใช้เซลล์ต้นกำเนิดพลูริโพเทนท์ (IPSCs) ในทางการแพทย์
ข้อดีของ iPSC คืออะไร?
iPSCs มีข้อดีกว่าสเต็มเซลล์ประเภทอื่นหลายประการ เนื่องจากสามารถสร้าง iPSC จากเซลล์ของผู้ป่วยเอง จึงช่วยลดความเสี่ยงของการถูกปฏิเสธของภูมิคุ้มกันเมื่อนำไปใช้ในการรักษา วิธีการเฉพาะบุคคลนี้อาจนำไปสู่การรักษาที่มีประสิทธิภาพและตรงเป้าหมายสำหรับผู้ป่วยแต่ละราย iPSC ยังหลีกเลี่ยงข้อกังวลด้านจริยธรรมที่เกี่ยวข้องกับการใช้เซลล์ต้นกำเนิดจากตัวอ่อน ข้อดีอีกประการหนึ่งคือความสามารถในการกำหนดเป้าหมายของยีน การปรับเปลี่ยนการกลายพันธุ์ที่ก่อให้เกิดโรคให้เป็นลำดับจีโนมปกติ เนื่องจากความเก่งกาจของพวกมัน iPSCs สามารถนำไปและแยกความแตกต่างในเซลล์ประเภทใดก็ได้ในร่างกาย ทำให้เป็นเครื่องมือที่น่าสนใจสำหรับเวชศาสตร์ฟื้นฟูและการสร้างแบบจำลองโรค
เมทริกซ์นอกเซลล์ – ปัจจัยสำคัญในการเพาะเลี้ยง iPSC
MEFs หรือไฟโบรบลาสต์ตัวอ่อนของหนูมักใช้เป็นชั้นป้อนในการเพาะเลี้ยง iPSC MEFs เป็นเซลล์เนื้อเยื่อเกี่ยวพันชนิดหนึ่งที่ได้มาจากระยะเอ็มบริโอของหนู และโดยทั่วไปจะใช้เป็นชั้นป้อนเพื่อรองรับการเจริญเติบโตและความแตกต่างของ iPSC MEF ทำหน้าที่เป็นแหล่งที่มาของปัจจัยการเจริญเติบโตที่จำเป็นและโมเลกุลอื่นๆ ที่ iPSC จำเป็นต้องเติบโตและสร้างความแตกต่าง
แม้ว่าโดยทั่วไปจะใช้ MEFs เป็นเลเยอร์ฟีดเดอร์สำหรับวัฒนธรรม iPSC แต่ก็มีข้อจำกัดบางประการสำหรับแนวทางนี้ ตัวอย่างเช่น MEF อาจเตรียมและบำรุงรักษาได้ยาก และมีความเสี่ยงที่จะปนเปื้อนเชื้อโรคหรือเซลล์ที่ไม่ต้องการอื่นๆ นอกจากนี้ การใช้ชั้นอาหารที่ได้จากสัตว์ทำให้เกิดข้อกังวลด้านจริยธรรมและอาจจำกัดการใช้ iPSC ทางคลินิกในมนุษย์
Matrigel เป็นอีกหนึ่งเมทริกซ์นอกเซลล์ (ECM) ที่ใช้กันทั่วไปในวัฒนธรรม iPSC เป็น ECM ที่มีจำหน่ายทั่วไปซึ่งได้มาจากเซลล์มะเร็งของเมาส์และมีส่วนผสมของโปรตีน ECM ที่ซับซ้อน รวมทั้ง laminin, collagen IV และ heparan sulfate proteoglycans แม้ว่า Matrigel จะมีประสิทธิภาพสูงในการสนับสนุนการเติบโตและความแตกต่างของ iPSC แต่ก็มีข้อจำกัดบางประการ เนื่องจากได้มาจากเซลล์ซาร์โคมาของหนู องค์ประกอบของมันจะแตกต่างกันไปในแต่ละล็อตและอาจมีปัจจัยที่ไม่รู้จักซึ่งอาจมีอิทธิพลต่อพฤติกรรมของ iPSC และอาจส่งผลต่อความสามารถในการทำซ้ำของผลลัพธ์ เช่นเดียวกับ MEFs การใช้ผลิตภัณฑ์ที่ได้จากสัตว์ในวัฒนธรรมของ iPSC ทำให้เกิดความกังวลด้านจริยธรรมและอาจจำกัดการใช้งานทางคลินิกของ iPSC
iMatrix-511 ปรับปรุงวัฒนธรรม iPSC
Laminin-511 เป็นองค์ประกอบหลักของ ECM และพบว่ามีบทบาทสำคัญในวัฒนธรรมของ iPSC แม้จะเป็น ECM ที่สำคัญสำหรับการเพาะเลี้ยง iPSC แต่ laminin-511 ก็ไม่เหมาะสำหรับการผลิตจำนวนมาก เนื่องจากมีน้ำหนักโมเลกุลที่ใหญ่และมีลักษณะเป็นเฮเทอโรไตรเมอร์ ด้วยเหตุนี้ กลุ่มของ Prof. Sekiguchi จึงพัฒนาและผลิตชิ้นส่วนรีคอมบิแนนท์ของ laminin-511 (ชิ้นส่วน E8) ที่คงฤทธิ์การจับตัวของอินทิกรินของ laminin-511 ที่ไม่บุบสลายไว้อย่างสมบูรณ์
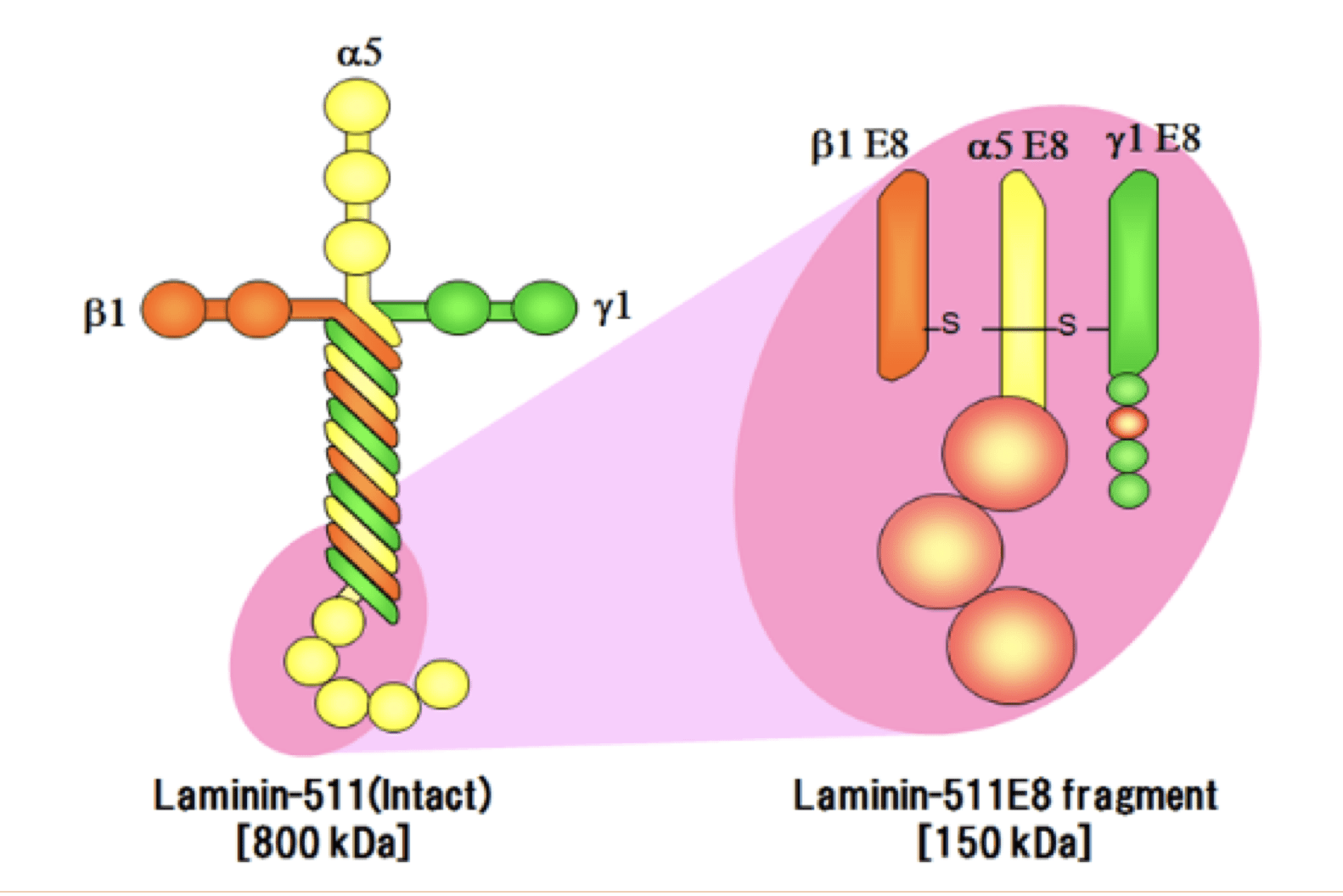 ลามิเนตแบบเต็มความยาว (ไม่บุบสลาย) และลามิเนตที่ถูกตัดทอน (ชิ้นส่วน E8)
ลามิเนตแบบเต็มความยาว (ไม่บุบสลาย) และลามิเนตที่ถูกตัดทอน (ชิ้นส่วน E8)
ส่วนรีคอมบิแนนต์ที่เรียกว่า 'ไอเมทริกซ์-511' มีข้อได้เปรียบที่สำคัญสองประการเหนือ laminin-511 ที่ไม่บุบสลาย ประการแรก เนื่องจากขนาดที่เล็กกว่า ทำให้ iMatrix-511 สามารถผลิตในปริมาณมากได้ง่ายกว่า laminin-511 ที่ไม่บุบสลาย ประการที่สอง iMatrix-511 มีศักยภาพมากกว่า laminin-511 ที่ไม่บุบสลายเพื่อรักษาการยึดเกาะและการขยายตัวของเซลล์ต้นกำเนิดหลายเซลล์ของมนุษย์หลังจากการแยกตัวของเซลล์เดียว
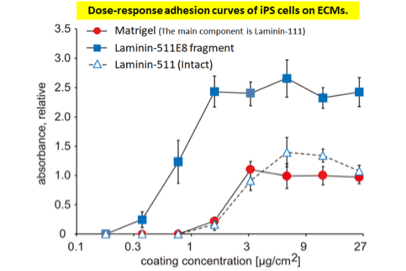 iPSC ของมนุษย์ยึดติดกับชิ้นส่วน Laminin-511 E8 อย่างแน่นหนามากกว่าชิ้นส่วน Laminin-511 (สภาพสมบูรณ์) หรือ Matrigel มิยาซากิ เอตอัล ณัฐคอมมิชชัน https://doi.org/10.1038/ncomms2231 (ข้อมูลเพิ่มเติม)*ตัวเลขมีการแก้ไขบางส่วน
iPSC ของมนุษย์ยึดติดกับชิ้นส่วน Laminin-511 E8 อย่างแน่นหนามากกว่าชิ้นส่วน Laminin-511 (สภาพสมบูรณ์) หรือ Matrigel มิยาซากิ เอตอัล ณัฐคอมมิชชัน https://doi.org/10.1038/ncomms2231 (ข้อมูลเพิ่มเติม)*ตัวเลขมีการแก้ไขบางส่วน
iMatrix-511 ยังสามารถใช้ใน “วิธีการผสมล่วงหน้า” ซึ่งไม่จำเป็นต้องเคลือบสีล่วงหน้าก่อนการเพาะเซลล์ และต้องใช้ iMatrix-511 เพียงครึ่งเดียว วิธีการใหม่ในการใช้ iMatrix-511 รองรับการยึดเกาะของเซลล์และการขยายตัวในระยะยาวเมื่อเทียบกับวิธีการเคลือบผิวล่วงหน้า ช่วยให้การบำรุงรักษา hPSCs มีค่าใช้จ่ายน้อยลงและใช้เวลาน้อยลง
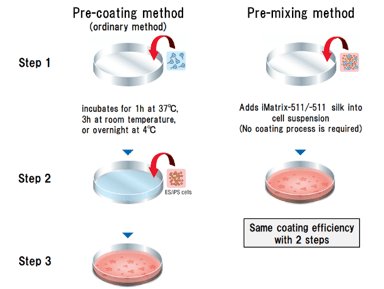 เปรียบเทียบ “วิธีเคลือบสีล่วงหน้า” กับ “วิธีผสมล่วงหน้า”
เปรียบเทียบ “วิธีเคลือบสีล่วงหน้า” กับ “วิธีผสมล่วงหน้า”
นอกเหนือจาก iPSCs แล้ว iMatrix-511 ยังสามารถใช้กับ hESC และเซลล์ปฐมภูมิของมนุษย์ได้ iMatrix-511 ถูกใช้อย่างแพร่หลายโดยนักวิจัยหลายคนและได้รับการตีพิมพ์ในหลายๆ บทความที่ผ่านการตรวจสอบโดยเพื่อน. iMatrix-511 มีจำหน่ายในเกรดทางคลินิกซึ่งตรงตามมาตรฐานของส่วนผสมทางชีวภาพโดย Pharmaceutical and Medical Devices Agency (PMDA) ซึ่งเป็นหน่วยงานรัฐบาลในประเทศญี่ปุ่นที่คล้ายคลึงกับ FDA กฎระเบียบนี้เป็นหนึ่งในกฎระเบียบที่เข้มงวดที่สุดในโลก และ iMatrix-511MG ไม่เพียงแต่ตอบสนองข้อกำหนดด้านกฎระเบียบเท่านั้น แต่ยังถูกนำไปใช้กับการใช้งานทางคลินิกที่มีชื่อเสียงจำนวนมากในประเทศญี่ปุ่น รวมถึงการปลูกถ่าย แผ่นเซลล์เยื่อบุผิวกระจกตา. iMatrix-511 ทางคลินิกยังเข้ากันได้กับ GMP ซึ่งช่วยให้สามารถเคลื่อนย้ายจากการวิจัยขั้นพื้นฐานได้อย่างราบรื่นโดยใช้ iMatrix-511to ทางคลินิกเกรด RUO โดยรวมแล้ว iMatrix-511 เป็นเครื่องมืออันทรงพลังที่ช่วยอำนวยความสะดวกในการเติบโตและอัตราการรอดชีวิตของเซลล์สูง ทำให้วัฒนธรรมของ iPSC เรียบง่ายและเชื่อถือได้!
อ้างอิง
มิยาซากิ, ต., ฟุตากิ, เอส., ซูเอโมริ, เอช. เอตอัล ชิ้นส่วน Laminin E8 สนับสนุนการยึดเกาะที่มีประสิทธิภาพและการขยายตัวของเซลล์ต้นกำเนิดหลายเซลล์ของมนุษย์ที่แยกตัวออกจากกัน ณัฐคอมมิชชัน 3, 1236 (2012) https://doi.org/10.1038/ncomms2231
มิยาซากิ, ที., อิโซเบะ, ที., นาคัตสึจิ, เอ็น. เอตอัล วัฒนธรรมการยึดเกาะที่มีประสิทธิภาพของสเต็มเซลล์มนุษย์ที่มีศักยภาพสูงโดยใช้ชิ้นส่วนลามินในลักษณะที่ไม่เคลือบผิว Sci Rep 7, 41165 (2017). https://doi.org/10.1038/srep41165
โมราดี, S., มาห์ดิซาเดห์, เอช., Šarić, T. เอตอัล การวิจัยและการบำบัดด้วยสเต็มเซลล์ที่ชักนำให้เกิดพลูริโพเทนต์ (iPSCs): ข้อพิจารณาทางสังคม กฎหมาย และจริยธรรม สเต็มเซลล์เรสเธอ 10, 341 (2019). https://doi.org/10.1186/s13287-019-1455-y
[/ Vc_column_text] [/ vc_column] [/ vc_row]